Si revisamos la bibliografía sabemos que el enfoque del shock cardiogénico (SC) estaba en el infarto agudo de miocardio (IAM); la subsecuente disfunción ventricular generada por la injuria isquémica es la causa del 80% de los casos de shock cardiogénico en este escenario y éste se presenta en el 5-15% de pacientes con IAM 1
Si revisamos la bibliografía sabemos que el enfoque del shock cardiogénico (SC) estaba en el infarto agudo de miocardio (IAM); la subsecuente disfunción ventricular generada por la injuria isquémica es la causa del 80% de los casos de shock cardiogénico en este escenario y éste se presenta en el 5-15% de pacientes con IAM 1 .
¿“Hemos fracasado” al intentar reducir la mortalidad? Las cifras se mantienen en dos dígitos, 50% aproximadamente2,3. El último resultado exitoso en este escenario fue el de la revascularización, lo aprendimos del SHOCK trial. Desde 1999 no teníamos un resultado como el que nos demuestra DanGer-SHOCK 4.
Una de las revoluciones que hemos tenido en el último tiempo es la visión en la detección del shock cardiogénico, pasamos de pensar que todo es igual y existe una sola medida para todos, a intentar comprender su amplio espectro, no sólo mediante la etiología si no mediante los fenotipos; sin duda SCAI3 es el gran contribuyente que nos obliga a reinterpretar la literatura. La mortalidad en shock cardiogénico no es igual, sin embargo, es bien conocido que si el desencadenante es un evento coronario agudo nada bueno se avecina. Fue el primer straight necesario en este camino; pero ¿es suficiente? Probablemente un estudio randomizado no tendremos en este aspecto, el arte de la medicina estará plasmado en lo que hemos reaprendido. La clasificación SCAI.
Hace unos pocos días se presentó en el congreso del ACC 2024 los resultados de uno de los estudios más esperados en el área de cuidado crítico cardíaco DanGer-Shock4, esperado por una década.
Centrémonos en DanGer Shock exclusivamente:
Es un estudio abierto, duró 10 años, participaron 14 centros de Dinamarca, Alemania y del Reino Unido, analizó datos de 355 (1211 screening) pacientes que presentaron STEMI (infarto agudo de miocardio con elevación del ST) y evolucionaron con shock cardiogénico.
Diseño del estudio:
Asignación al azar 1:1
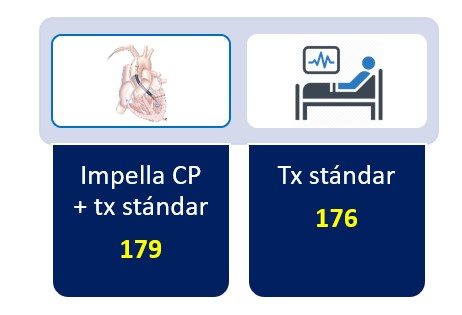
Impella CP debía ser implantado inmediatamente después de la aleatorización y su funcionamiento fue establecido al nivel más alto de rendimiento durante al menos 48 horas, salvo que exista complicaciones.
En caso de inestabilidad hemodinámica: escalar a otro soporte circulatorio mecánico adicional, esto podía ser después de la aleatorización en cualquiera de los grupos del ensayo.
Opciones recomendadas:
Grupo Impella CP a impella 5.0, Impella RP o ECMOVA
Grupo cuidado stándard a ECMO VA, aunque se permitió el uso de Impella 5.0
Criterios de inclusión & exclusión:


Uso de otros dispositivos:

Resultados principales:
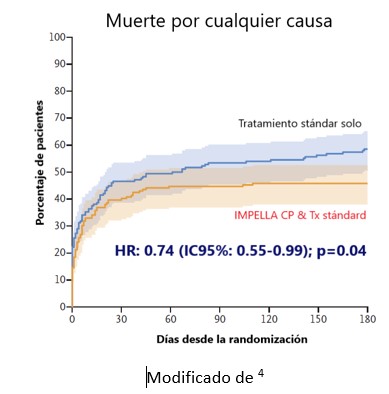
Mortalidad por todas las causas a los 6 meses para Impella CP + atención estándar vs atención estándar: 8 % vs 58.5 % (HR: 0.74; IC95%: 0.55-0.99; p = 0.04).
Resultados secundarios:
-Compuesto a los 6 meses (aumento del tratamiento a soporte circulatorio mecánico adicional temporal, trasplante de corazón o muerte por cualquier causa) 52.5 % vs a 63.6 % (HR: 0.72; IC95%: 0.55-0.95)
-Valoración de seguridad (hemorragia grave, isquemia de la extremidad, hemólisis, fallo del dispositivo o empeoramiento de la insuficiencia aórtica) 24.0 % vs 6.2 % (HR: 4.74; IC95%: 2.36-9.55)
-Sangrado moderado o severo: 21.8% vs. 11.9% (p < 0.05)
-Isquemia de las extremidades: 5.6% vs 1.1% (p < 0.05)
-Requerimiento de diálisis: 41.9% vs. 26.7% (p < 0.05)
-Sepsis con hemocultivo positivo: 11.7% vs. 4.5% (p < 0.05)
Conclusión del estudio:
La implantación rutinaria de Impella CP más la atención estándar es superior a la atención estándar sola para reducir la mortalidad a los 6 meses en pacientes que presentan STEMI y shock cardiogénico; aunque tienen mayor riesgo de complicaciones.
COMENTARIO:
Sin duda, celebramos un resultado positivo en este grupo de pacientes, especialmente considerando la reciente falta de evidencia a favor. El estudio ECLS-Shock5 ha suscitado interrogantes sobre el uso de la ECMO-VA en este contexto, así como sobre el balón de contrapulsación6, el uso rutinario de los dos dispositivos no ha demostrado beneficios. Aunque este resultado nos llena de entusiasmo, la mortalidad sigue siendo elevada, rondando el 60% en el grupo control, lo cual es preocupante dado el contexto actual. Es relevante señalar que el reclutamiento de pacientes tomó diez años (de enero de 2013 a julio de 2023) para alcanzar una muestra de 355, lo que sugiere que la selección de los participantes podría haber sido determinante.
Comparando con estudios previos como el ECLS-Shock, que incluyó un alto porcentaje de pacientes con parada cardíaca extrahospitalaria, frente al DanGer-Shock que tuvo una proporción significativamente menor (77.5% vs 21.8%), es evidente la importancia de la selección. Además, al considerar biomarcadores como el lactato arterial, se observan diferencias entre los dos estudios (4.5 mmol/L DanGer-shock vs 6.8 mmol/L ECLS-Shock), lo que sugiere que la bomba microaxial podría estar abordando un problema diferente al lactato elevado por la parada cardíaca.
Es crucial tener en cuenta la posible influencia de la falta de terapias avanzadas, como el trasplante o los dispositivos de asistencia ventricular izquierda (LVAD), en la mortalidad del ECLS-Shock. Estas opciones si fueron contempladas en el DanGer-Shock.
Las complicaciones observadas deben interpretarse en el contexto adecuado. Por ejemplo, el aumento en la necesidad de diálisis podría estar relacionado con el manejo Impella CP (en el protocolo se establece a 8 RPM) que puede aumentar el riesgo de hemólisis o la prolongación de la vida de los pacientes tratados podría haber contribuido a la aparición de estas complicaciones, lo que debe tenerse en cuenta también al evaluar la estancia en unidades de cuidados intensivos. Es fundamental analizar la mortalidad considerando el riesgo competitivo y determinar si las complicaciones tienen un impacto significativo en la mortalidad a largo plazo. Además, el análisis a 180 días podría haber influido en el resultado positivo, aunque las curvas de supervivencia se separen cerca de los 30 días. Los números sugieren un NNT de 8 y un NNH de 6, pero el intervalo de confianza del resultado deja cierta incertidumbre sobre la magnitud precisa del beneficio.
Es importante señalar que solo el 21% de los participantes fueron mujeres, y el análisis de subgrupos preespecificados no mostró beneficios para este grupo. Se requiere un análisis más detallado, especialmente para evaluar el impacto de los efectos adversos, ya que los datos presentados hasta ahora son limitados en este aspecto.

El resultado en global nos anima a pensar que los beneficios superan los riesgos y que la selección es clave, pero ¿es suficiente para estandarizar el uso rutinario de Impella CP en el shock cardiogénico secundario a STEMI? No. La magnitud del beneficio es incierta, la estricta selección de pacientes y la regionalización son factores para considerar. La evolución de los dispositivos probablemente sea exponencial para reducir el riego de complicaciones que no sabemos cómo impactarán a largo plazo, y no un detalle menor, ¿todos disponemos de Impella CP para tratar el shock cardiogénico en STEMI? Por ahora debemos partir del reaprendizaje en el reconocimiento y diagnóstico del shock cardiogénico, de la estandarización del manejo apoyados en la evidencia. Es necesario continuar en la búsqueda de la reducción de la mortalidad y reconfirmar este resultado, que después de 25 años nos deja lecciones, preguntas, pero la positividad que merece ser reconocida.
Ver link AQUI
BIBLIOGRAFIA
1.Reynolds HR, Hochman JS. Cardiogenic shock current concepts and improving outcomes. Circulation. 2008;117(5):686–97.
2.Berg DD, Bohula EA, Van Diepen S, Katz JN, Alviar CL, Baird-Zars VM, et al. Epidemiology of Shock in Contemporary Cardiac Intensive Care Units. Circ Cardiovasc Qual Outcomes [Internet]. 2019 Mar 1 [cited 2024 Apr 18];12(3). Available from: https://www.ahajournals.org/doi/abs/10.1161/CIRCOUTCOMES.119.005618
3.Hill KL, Rustin MA, Asche MA, Bennett CE, Patel PC, Jentzer JC. Cardiogenic Shock Classification and Associated Mortality Risk. Vol. 98, Mayo Clinic Proceedings. Elsevier Ltd; 2023. p. 771–83.
4.Møller JE, Engstrøm T, Jensen LO, Eiskjær H, Mangner N, Polzin A, et al. Microaxial Flow Pump or Standard Care in Infarct-Related Cardiogenic Shock. N Engl J Med [Internet]. 2024 Apr 7; Available from: http://www.ncbi.nlm.nih.gov/pubmed/38587239
5.Thiele H, Zeymer U, Akin I, Behnes M, Rassaf T, Mahabadi AA, et al. Extracorporeal Life Support in Infarct-Related Cardiogenic Shock. New England Journal of Medicine [Internet]. 2023 Aug 26; Available from: http://www.nejm.org/doi/10.1056/NEJMoa2307227
6.Thiele H, Zeymer U, Neumann FJ, Ferenc M, Olbrich HG, Hausleiter J, et al. Intraaortic Balloon Support for Myocardial Infarction with Cardiogenic Shock. New England Journal of Medicine. 2012 Oct 4;367(14):1287–96.