El deterioro de la función sistólica del ventrículo izquierdo (VI) es reconocido por ser un resultado adverso de la sobrecarga de presión en una estenosis aórtica (EAo) severa. La respuesta natural ante ésta patología es el remodelado concéntrico y el aumento de la masa ventricular con el objetivo de mantener la tensión parietal y el
El deterioro de la función sistólica del ventrículo izquierdo (VI) es reconocido por ser un resultado adverso de la sobrecarga de presión en una estenosis aórtica (EAo) severa. La respuesta natural ante ésta patología es el remodelado concéntrico y el aumento de la masa ventricular con el objetivo de mantener la tensión parietal y el volumen sistólico. Sin embargo, con la progresión de la enfermedad se produce un aumento del espacio intersticial con fibrosis difusa (potencialmente reversible) y posteriormente muerte celular con fibrosis de reemplazo (irreversible).1 Se cree que éstos mecanismos se encuentran vinculados con la aparición de síntomas, insuficiencia cardíaca y eventos cardiovasculares adversos, incluso posteriores al reemplazo de la válvula aórtica (RVAo). Un diagnóstico temprano de una disfunción ventricular permite seleccionar el momento adecuado de la intervención valvular. Ésta revisión busca definir si existe un punto de corte óptimo de la fracción de eyección del VI (FEVI) para definir disfunción sistólica en pacientes con EAo o si debe ser reemplazada su uso por el strain global longitudinal (GLS).
Umbral incorrecto de la FEVI para las intervenciones
Las principales guías recomiendan el RVAo en pacientes asintomáticos con FEVI menor al 50% (clase I, nivel B en AHA/ACC y nivel C en ESC).2,3 Sin embargo, éste punto de corte merece un minucioso análisis:
- Las guías internacionales consideran como disfunción del VI un valor de FEVI menor a 52% en hombres y 54% en mujeres. Sin embargo, no se ha modificado el punto de corte de 50% en las guías de valvulopatía aórtica.
- EAo severa asintomática con FEVI < 50% es un escenario es poco habitual, con una prevalencia del 0.4%, ya que la vasta mayoría de los pacientes desarrollan síntomas antes de una reducción de la FEVI.4 Pero los pacientes pueden adaptar su estilo de vida al reducir su capacidad funcional y esto genera dificultades para establecer si son verdaderamente “asintomáticos”.
- La estrategia basada en esperar hasta que la su FEVI sea <50% lleva a desenlaces subóptimos tanto en el intraquirúrgico como en el postoperatorio.
La FEVI es un fuerte predictor de mortalidad, independientemente de la presencia de síntomas, y la misma se incrementa a partir de valores menores a 60%. Dahl y col. demostraron que las tasas de mortalidad de los pacientes sometidos a RVAo varían según la FEVI del preoperatorio. Pacientes con <50% de FEVI tienen una mortalidad a 5 años del 41%, aquellos con FEVI entre 50-59% del 35%, con FEVI entre 60-69% del 26% y con FEVI ≥70% del 22%. Los pacientes con FEVI ≥60% tienen un resultado similar.5
Corroborando éstos hallazgos, Ito y col. demostraron una mayor mortalidad en pacientes con FEVI 50-59% frente a aquellos con FEVI ≥60%, independientemente si eran sometidos a RVAo.6 A su vez, éste estudio evidenció que la FEVI comienza a disminuir incluso antes de que la EAo se encuentre en rango de severidad.
Por todo lo expuesto, el valor umbral de FEVI < 50% para indicar intervención es demasiado bajo. Una FEVI umbral <60% sería más adecuado.
Rol del GLS en la detección de la disfunción subclínica del VI
A pesar del uso universal de la FEVI, ésta tiene importantes limitaciones. Es dependiente de las cargas y presenta una variabilidad intra e interobservador entre un 8-10%. A su vez, la FEVI puede mantenerse en rangos “normales” a pesar de una reducción de la contractilidad miocárdica, mediante el uso de reserva de precarga o de cambios en la geometría ventricular, por lo tanto no es un buen marcador de disfunción “subclínica”.7
El uso del GLS del VI proporciona una cuantificación semiautomática de la deformidad miocárdica y puede ser un marcador precoz de disfunción subclínica del VI. Presenta una menor variabilidad intra e interobservador (5% y 8% respectivamente) que la FEVI. Sin embrago, también es dependiente de las cargas.
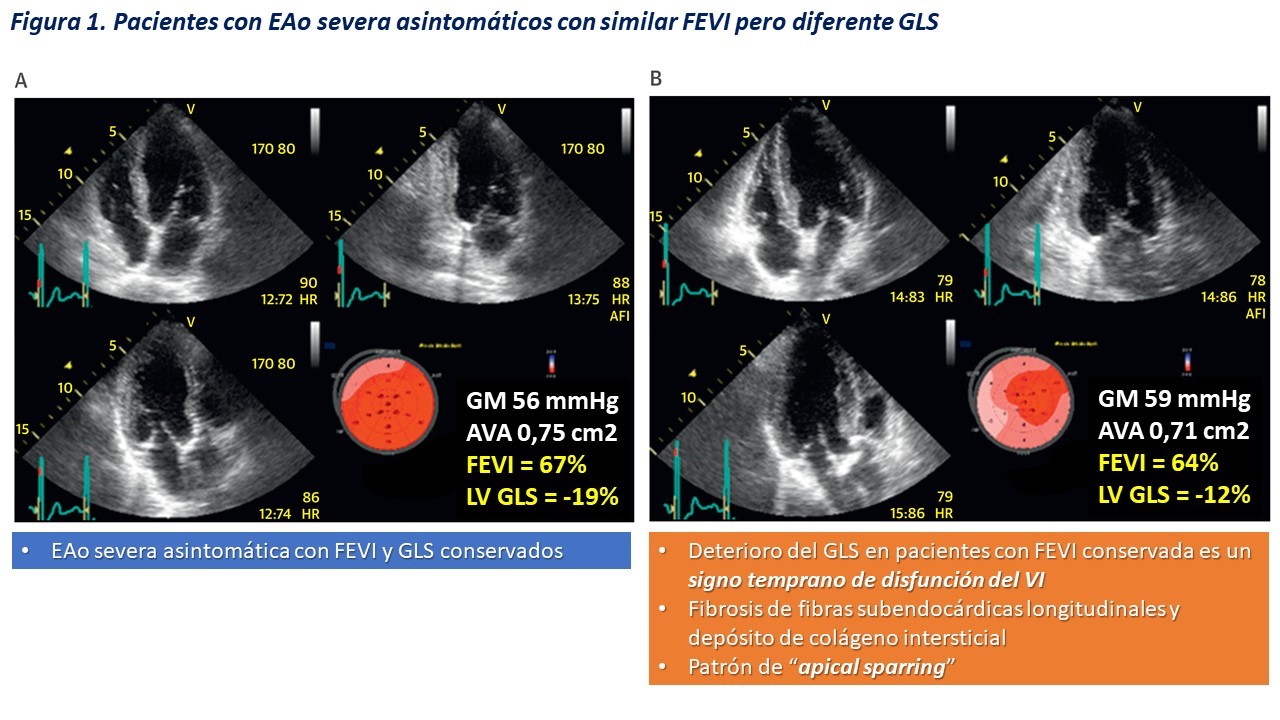
La depresión del GLS en pacientes con EAo severa y FEVI conservada es un signo temprano de disfunción del VI y se atribuye a la fibrosis de las fibras longitudinales del subendocardio y al depósito de colágeno intersticial. La fibrosis suele ser mayor en las bases que en el ápex, lo que genera un patrón de “conservación apical” (apical sparring) en el GLS (figura 1).
El grado de deterioro del GLS empeora a medida que la EAo se vuelve más grave, en contraste con la reducción tardía de la FEVI. Un GLS disminuido se asocia a necesidad de intervención valvular, eventos cardiovasculares en el postoperatorio y supervivencia, independientemente de la FEVI y de los síntomas del paciente.
La resonancia magnética cardíaca (RMC) ha brindado nuevos conocimientos con respecto a la disfunción del VI en la EAo. La presencia de realce tardío de gadolinio (LGE) se ha identificado en pacientes con diversos grados de severidad de EAo, a pesar de una FEVI normal. Además, el uso del tiempo de relajación de la magnetización longitudinal miocárdica (native T1 time) permite una evaluación más precisa de los cambios difusos del espacio intersticial. Un porcentaje significativo de pacientes presentan FEVI normal pero con LGE y valores elevados de T1. Datos actuales demuestran que a FEVI no diferencia efectivamente la fibrosis difusa de la fibrosis de reemplazo y por lo tanto no proporciona una evaluación adecuada de los cambios morfológicos y funcionales del VI.
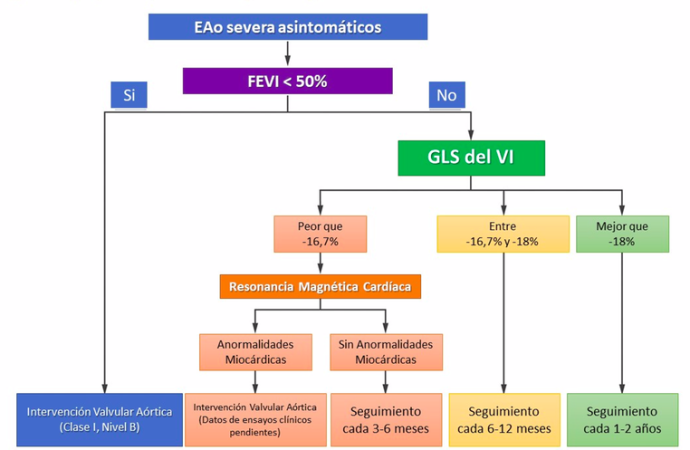
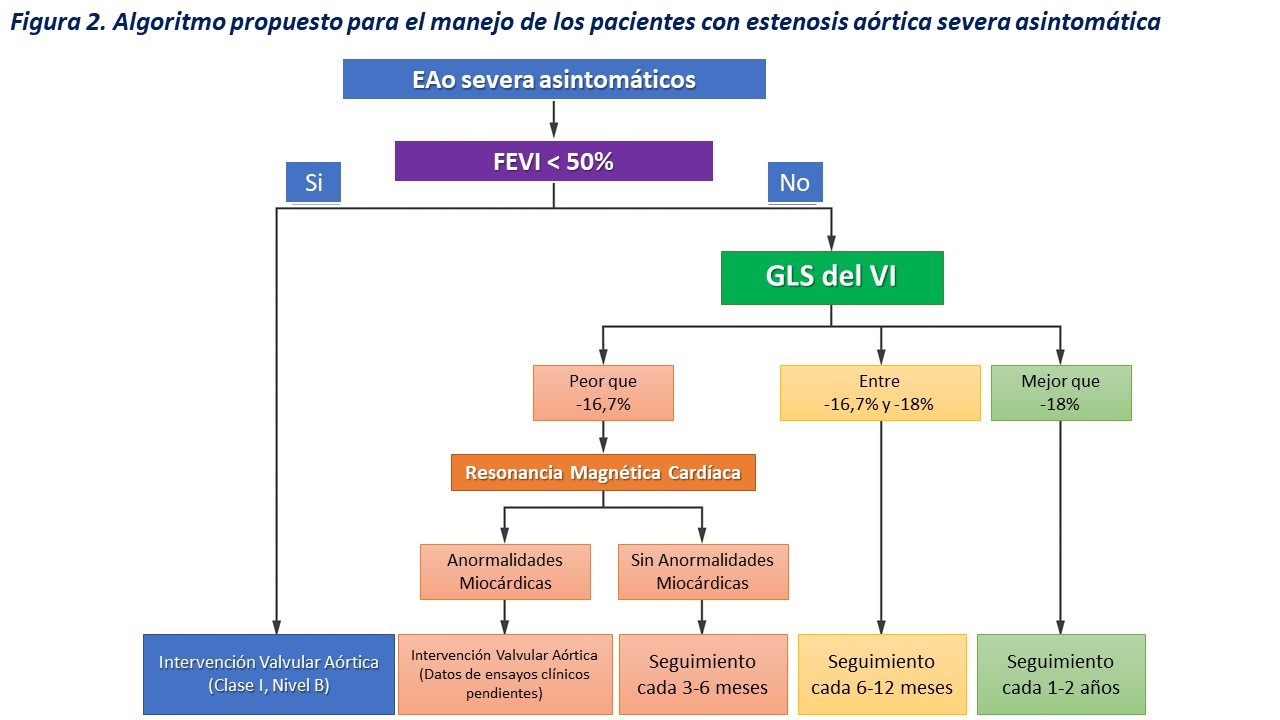
Los autores de ésta revisión proponen un algoritmo para ser utilizado en pacientes con EAo severa asintomática con FEVI conservada (figura 2).
Comentario personal
La indicación de intervenir a los pacientes asintomáticos con EAo severa y deterioro de la función sistólica del VI, definida como FEVI <50%, debería ser modificada. Es un valor de corte sumamente bajo, donde ya existe fibrosis miocárdica irreversible, con un muy pobre pronóstico independientemente del reemplazo valvular. ¿Debemos plantearnos cambiar el valor de corte de la FEVI o utilizar otro método para el diagnóstico precoz de disfunción? La FEVI es la medida de evaluación de la función sistólica más ampliamente utilizada para la evaluación cardíaca y valvular, se puede evaluar por múltiples modalidades de imágenes y es un fuerte predictor de mortalidad independientemente de los síntomas del paciente. En los últimos meses se ha publicado vasta evidencia que establece que los pacientes con EAo severa con FEVI menor al 60% tienen peor pronóstico, independientemente de que sean intervenidos.6,8,9 Por lo cual, deberíamos considerar éste valor como sinónimo de disfunción sistólica del VI e indicar la intervención valvular tomando éste como punto umbral.
Con respecto al uso de GLS del VI, es una valiosa herramienta, complementaria a la FEVI en la evaluación de los pacientes con EAo severa asintomáticos. A pesar de estar influenciada por la precarga y la poscarga, es lo suficientemente sensible para desenmascarar alteraciones miocárdicas estructurales y funcionales del VI, que la FEVI no puede revelar. Un metaanálisis reciente demuestra una fuerte relación entre un GLS del VI reducido y mortalidad por todas las causas en pacientes asintomáticos con EAo severa y FEVI preservada.10 Éstos resultados apoyan la utilización sistemática de ésta herramienta para la estratificación del riesgo y el manejo de éstos pacientes. A su vez, promueve su uso en la práctica clínica como un parámetro aditivo para la toma de decisiones. Un valor < -14.7% podría considerarse para futuras investigaciones como un umbral de disfunción precoz del VI. Sin embargo, debemos tener presenta que para su uso se requiere una buena calidad de imagen y un dedicado software que no es accesible en todos los laboratorios de ecocardiografía. A su vez, existe cierta controversia respecto a la variabilidad entre los resultados del GLS entre los diferentes equipos.
Con respecto a la evaluación por RMC, no parece ser una opción factible por el creciente número de pacientes con EAo, por lo cual se necesita una alternativa viable y de menor costo.
La hipótesis plantea en ésta revisión suena prometedora, pero debería ser evaluada en estudios prospectivos antes de ser integrada en las guías de recomendación.10-11
Referencias
- Bing R, Cavalcante JL, Everett RJ, et al. Imaging and Impact of Myocardial Fibrosis in Aortic Stenosis. J Am Coll Cardiol Img 2019;12:283–
- Baumgartner H, Falk V, Bax J, et al. Guia ESC/EACTS 2017 sobre el tratamiento de las valvulopatias. Rev Esp Cardiol. 2018;71(2):110.e1-e47.
- Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease. J Am Coll Cardiol 2014;63:2438–
- Henkel D, Maalouf J, Connolly H, et al. Asymptomatic left ventricular systolic dysfunction in patients with severe aortic stenosis: characteristics and outcomes. J Am Coll Cardiol 2012;60:2355–
- Dahl J, Eleid M, Michelena H, et al. Effect of left ventricular ejection fraction on postoperative outcome in patients with severe aortic stenosis undergoing aortic valve replacement. Circ Cardiovasc Imaging 2015;8:e002917.
- Ito S, Miranda WR, Nkomo VT, et al. Reduced left ventricular ejection fraction in patients with aortic stenosis. J Am Coll Cardiol 2018;71:1313–
- Aurigemma GP, Silver KH, Priest MA, Gaasch WH. Geometric changes allow normal ejection fraction despite depressed myocardial shortening in hypertensive left ventricular hypertrophy. J Am Coll Cardiol 1995;26:195–
- Lancellotti P, Magne J, Dulgheru R, et al. Outcomes of Patients With Asymptomatic Aortic Stenosis Followed Up in Heart Valve Clinics. JAMA Cardiol. 2018;3(11):1060-1068.
- Taniguchi T, Morimoto T, Shiomi H, et al. Prognostic Impact of Left Ventricular Ejection Fraction in Patients With Severe Aortic Stenosis. JACC Cardiovasc Interv.2018 Jan 22;11(2):145-157.
- Magne J, Cosyns B, Popescu B, et al. Distribution and Prognostic Significance of Left Ventricular Global Longitudinal Strain in Asymptomatic Significant Aortic Stenosis. An Individual Participant Data Meta-Analysis. J Am Coll Cardiol Img 2019;12:84–
- Vollema E, Sugimoto T, Shen M, et al. Association of Left Ventricular Global Longitudinal Strain With Asymptomatic Severe Aortic Stenosis Natural Course and Prognostic Value. JAMA Cardiol.2018 Sep 1;3(9):839-847.









































Deje un comentario
Registrese para comentar. Sus e-mail no será publicados