¿Es suficiente el resultado del estudio CULPRIT-SHOCK para que sea una recomendación Clase III? Introducción: Hasta el año 2017 la Sociedad Europea de Cardiología indicaba la realización de angioplastia multivaso en el infarto con shock cardiogénico, con un nivel de recomendación IIa, nivel de evidencia C (la opinión es favorable respecto de su utilidad o
¿Es suficiente el resultado del estudio CULPRIT-SHOCK para que sea una recomendación Clase III?
Introducción:
Hasta el año 2017 la Sociedad Europea de Cardiología indicaba la realización de angioplastia multivaso en el infarto con shock cardiogénico, con un nivel de recomendación IIa, nivel de evidencia C (la opinión es favorable respecto de su utilidad o eficacia). Sin embargo, ante la publicación de los resultados iniciales del estudio CULPRIT-SHOCK en el año 2018, dicha recomendación pasó a ser clase III – nivel de evidencia B (futilidad o potencial daño). [1]
La racionalidad fisiopatológica de realizar angioplastia multivaso en el shock cardiogénico es entre otros: disminuir la amenaza remota, el atontamiento y la hibernación, estabilizar otras placas inestables y con esto contribuir a mejorar el shock cardiogénico y reducir el deterioro de la función ventricular. Con la consiguiente reducción de la insuficiencia cardíaca en la evolución y de la mortalidad. Pero como contrapartida el procedimiento a varios vasos agrega el riesgo de complicaciones isquémicas, a veces derivadas de proceder lesiones que impresionan severas por espasmo y bajo flujo, pero que no lo son. Sumado al riesgo de intentar resolver oclusiones crónicas en un escenario agudo. Además del riesgo de sangrado, el retraso en el adecuado tratamiento médico y la nefropatía por contraste. Esta paridad de riesgos y beneficios se vio reflejada en los resultados de los metaanálisis que no indicaban que la estrategia multivaso fuera mejor que la de angioplastiar sólo al vaso considerado culpable.[2]
Comentario del artículo:
En el año 2017 se publican los resultados a 30 días del estudio CULPRIT-SHOCK, un multicéntrico, prospectivo, randomizado que incluyó pacientes con infarto y shock cardiogénico.[3] (Figura 1).
Figura 1. Diseño del CULPRIT SHOCK
El punto final primario combinado, mortalidad o progresión a la diálisis, fue favorable en forma significativa a la angioplastia sólo al vaso culpable. Lo mismo ocurrió con el punto final mortalidad total, motivando esto el cambio en la recomendación de la Sociedad Europea de Cardiología.
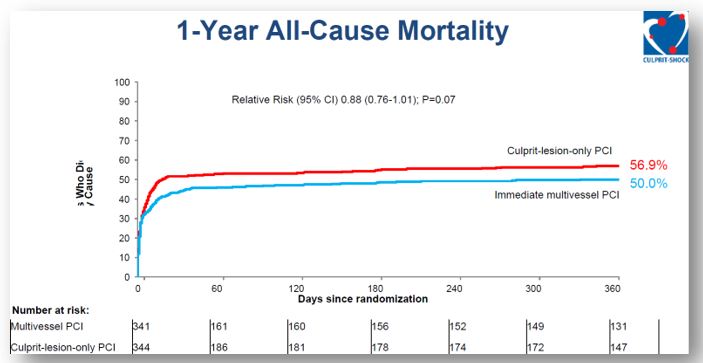
Recientemente en Agosto de 2018 fueron publicados los datos de seguimiento a un año de dicho estudio.[4] Si bien el punto final primario combinado se mantuvo favorable a la estrategia “sólo vaso culpable”, ninguno de sus componentes en particular mantuvo una diferencia significativa. El análisis exclusivo del punto final mortalidad total no fue significativamente diferente entre los grupos. (Figura 2).
Figura 2: Presentación del Dr. Holger Thiele en el congreso ESC 2018.
El estudio arrojó dos resultados favorables a la postura de revascularización multivaso inmediata: redujo las hospitalizaciones por insuficiencia cardíaca al año, así como también la necesidad de nuevos procedimientos de revascularización.
Comentarios y conclusiones personales:
En el shock cardiogénico los cardiólogos críticos buscamos como objetivos terapéuticos:
- a) reducir la mortalidad, b) el shock cardiogénico refractario y c) preservar la función ventricular para evitar la insuficiencia cardíaca a futuro. Sin embargo no suele ser nuestro objetivo principal evitar el daño renal que lleve a la diálisis, entendiendo que a veces es un precio que debemos pagar para salvarle la vida al paciente crítico. Además, el punto final “daño renal que lleva a diálisis” siempre irá en contra de la angioplastia multivaso, que utiliza más contraste que el tratamiento del vaso culpable solamente. Por lo que colocarlo dentro del punto final primario combinado es difícil de entender para un cardiólogo crítico.
Analizando en este estudio los objetivos puestos antes a consideración: vemos como la reducción de la mortalidad no mostró diferencias significativas entre ambas estrategias. Es más, la mayor diferencia no se observó en la mortalidad cardiovascular, sino en los eventos no cardíacos; fundamentalmente la muerte cerebral que fue mayor en el grupo multivaso, sin ser consecuencia directa de dicho tratamiento. La mitad de los pacientes del estudio ingresaron luego de haber sido reanimados de un paro cardíaco, un criterio de inclusión bastante opinable ya que se trata de una subpoblación muy especial en el grupo de los pacientes con shock.
Respecto del segundo punto, la evolución al shock cardiogénico refractario se presentó en el 60.8% de los pacientes con angioplastia multivaso y en el 66.3% del grupo que trató sólo la lesión culpable, sin que la diferencia alcance significación estadística.
Finalmente, la preservación de la función ventricular para evitar la insuficiencia cardíaca en la evolución fue favorable como hemos visto a la estrategia de revascularización multivaso.
Los sujetos incluidos en el CUPRIT-SHOCK no son exactamente el tipo de paciente con shock en los que piensa el cardiólogo crítico. La presión arterial media de la población incluida fue de 100/60 mm Hg (1/4 por encima de los 125 mm Hg de sistólica), el láctico fue normal en el 30% de los casos, se usaron inotrópicos no en todos sino en el 88% de los pacientes, asistencia ventilatoria en el 80%, 25% con oclusiones totales crónicas y 52% post paro cardíaco. Es más, si queremos transferir sus resultados a la población de Latinoamérica debemos tener en cuenta que en el 20% de los casos se usaron asistencias ventriculares más avanzadas que el balón de contrapulsación intraaórtico, lo que no refleja nuestra realidad.
Por todo lo comentado, no parecería apropiado abandonar completamente la estrategia de revascularización multivaso en los pacientes con shock cardiogénico, así como tampoco hacerla como rutina. En nuestra opinión sería más apropiado seleccionar para la estrategia multivaso a aquellos pacientes con mayor riesgo y potencial beneficio como ser: quienes tengan hipotensión refractaria, se encuentren con inotrópicos y asistencia ventilatoria mecánica, con lesiones críticas (>90%) proximales (especialmente en descendente anterior y tronco de coronaria izquierda), no trabajar sobre oclusiones totales, aquellos que no presenten hipercontractilidad compensadora en territorios remotos del infarto cuya arteria presente lesión, y en quienes se esté evaluando la colocación de una asistencia ventricular.
Es posible que los resultados al año del CULPRIT-SHOCK y el análisis venidero de diferentes subgrupos angiográficos modifiquen nuevamente la recomendación de las sociedades científicas sobre el tratamiento de revascularización del shock cardiogénico en el contexto del infarto.
Autores:
Dr. Horacio Fernandez
Jefe de Unidad Coronaria del Hospital Universitario Austral – Argentina.
Dr. José Santucci
Area de Insuficiencia Cardíaca Avanzada – Hospital Universitario Austral.
- – Ver link AQUI
[1] Neumann F-J, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. European Heart Journal [Internet]. 25 de agosto de 2018 [citado 23 de octubre de 2018]; Disponible en: https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehy394/5079120
[2] de Waha S, Jobs A, Eitel I, Pöss J, Stiermaier T, Meyer-Saraei R, et al. Multivessel versus culprit lesion only percutaneous coronary intervention in cardiogenic shock complicating acute myocardial infarction: A systematic review and meta-analysis. European Heart Journal: Acute Cardiovascular Care. febrero de 2018;7(1):28-37.
[3] Thiele, H., Akin, I., Sandri, M., Fuernau, G., de Waha, S., Meyer-Saraei, R., Nordbeck, P., Geisler, T., Landmesser, U., Skurk, C., Fach, A., Lapp, H., Piek, J.J., Noc, M., Goslar, T., Felix, S.B., Maier, L.S., Stepinska, J., Oldroyd, K., Serpytis, P., Montalescot, G., Barthelemy, O., Huber, K., Windecker, S., Savonitto, S., Torremante, P., Vrints, C., Schneider, S., Desch, S., Zeymer, U., 2017. PCI Strategies in Patients with Acute Myocardial Infarction and Cardiogenic Shock. New England Journal of Medicine 377, 2419–2432. https://doi.org/10.1056/NEJMoa1710261
[4] Thiele, H., Akin, I., Sandri, M., de Waha-Thiele, S., Meyer-Saraei, R., Fuernau, G., Eitel, I., Nordbeck, P., Geisler, T., Landmesser, U., Skurk, C., Fach, A., Jobs, A., Lapp, H., Piek, J.J., Noc, M., Goslar, T., Felix, S.B., Maier, L.S., Stepinska, J., Oldroyd, K., Serpytis, P., Montalescot, G., Barthelemy, O., Huber, K., Windecker, S., Hunziker, L., Savonitto, S., Torremante, P., Vrints, C., Schneider, S., Zeymer, U., Desch, S., 2018. One-Year Outcomes after PCI Strategies in Cardiogenic Shock. New England Journal of Medicine. https://doi.org/10.1056/NEJMoa1808788










































Deje un comentario
Registrese para comentar. Sus e-mail no será publicados