El Síndrome cardiorrenal (SCR) es un término abarcativo que describe la compleja interacción cardíaca y renal, cuya disfunción simultánea tanto sea aguda como crónica, inicia, perpetúa y/o acelera la enfermedad y el declive del otro. La disfunción renal es una de las co-morbilidades más importantes en los pacientes con Insuficiencia cardíaca (IC) crónica y se
El Síndrome cardiorrenal (SCR) es un término abarcativo que describe la compleja interacción cardíaca y renal, cuya disfunción simultánea tanto sea aguda como crónica, inicia, perpetúa y/o acelera la enfermedad y el declive del otro.
La disfunción renal es una de las co-morbilidades más importantes en los pacientes con Insuficiencia cardíaca (IC) crónica y se acentúa o se hace más evidente durante los episodios de insuficiencia cardiaca aguda (ICA). La prevalencia de SCR en los pacientes con insuficiencia cardíaca (IC) es de un 25-30%, universalmente asociado a peor pronóstico.
Definición y diagnóstico:
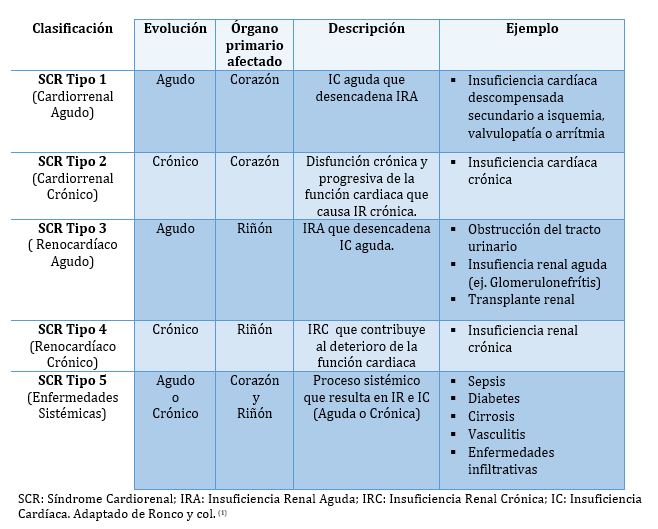
En la actualidad los pacientes con SCR se clasifican en 5 grupos (Ver Tabla 1). Las primeras cuatro categorías de SCR basan su clasificación en el órgano primario afectado y el tiempo de evolución. Mientras que la quinta está compuesto por los pacientes con SCR secundario a enfermedades sistémicas. (1,2)
Tabla 1.
A pesar de la orientación fisiopatológica de esta clasificación, y posterior a una década desde su implementación, al día de hoy no se logró grandes cambios en el abordaje clínico ni terapéutico de estos pacientes.
Es complejo diagnosticar y agrupar a los pacientes con SCR, primariamente, debido a la falta de una única definición de insuficiencia renal. Incluso en la historia de los estudios realizados en pacientes con insuficiencia cardíaca y disfunción renal, se utilizaron diversos parámetros para realizar diagnóstico de IR sea tanto como valores absolutos o porcentuales de creatinina y a pesar de que se haya propuesto unificar el criterio diagnóstico de IR, al día de hoy no se ha logrado.
En un intento de disminuir las disyuntivas diagnósticas, múltiples investigadores se vieron motivados a identificar biomarcadores que pudieran ser de utilidad para diagnosticar el SCR.
A pesar de los múltiples estudios con NGAL, KIM-1 y NAG, al momento los resultados continúan siendo heterogéneos, por lo que es necesario continuar con las investigaciones antes de sentenciar si son verdaderamente útiles para establecer el deterioro crónico de la función renal, eventualmente diferenciar la injuria tubular de un aumento aislado de la creatinina sin daño renal real, e identificar pacientes con daño tubular e insuficiencia cardíaca a pesar de valores de creatina normal.
Fisiopatología del Síndrome Cardiorrenal:
Los mecanismos fisiopatológicos responsables del SCR son complejos, multifactoriales y no del todo conocidos, los procesos hemodinámicos como el bajo gasto y la congestión venosa, están intrínsecamente relacionados, aunque no explican la totalidad de las consecuencias clínicas.
La activación persistente del sistema renina angiotensina aldosterona (SRAA), la sobre-estimulación simpática, los procesos de inflamación, fibrosis, y la desregulación del balance entre el oxido nítrico y los especies reactivas de oxígeno, interactúan entre sí y conllevan potencialmente a una peor función cardíaca y renal.
En consecuencia, la reducción del gasto cardiaco y la redistribución de la congestión producen disminución de la perfusión renal. La estimulación del sistema nervioso simpático, el sistema renina-angiotensina-aldosterona y la secreción de vasopresina conducen a una intensificación de la reabsorción de sodio y agua, en un intento de preservar la perfusión renal y el filtrado glomerular (FG), sin embargo, y a largo plazo, induce efectos deletéreos sobre el corazón y el riñón.
La activación del sistema renina-angiotensina-aldosterona tiene como finalidad mantener el FG en situaciones de hipoperfusión aguda; no obstante, su estimulación de modo persistente desempeña un papel clave en la lesión renal producida a través de una hipertrofia celular, una estimulación de la fibrosis, un estrés oxidativo y una activación de mecanismos inflamatorios.
Y por último, sumado a lo ante dicho, la actividad simpática elevada es un factor desencadenante reconocido en la descompensación de la IC, cambios agudos en la capacitancia venosa vascular esplácnica regulada por el tono simpático pueden dar lugar a una translocación brusca del volumen hacia la zona circulatoria efectiva, causando una sobrecarga venosa central.
Todos y cada uno de estos mecanismos están estrechamente relacionados y conectados. Generando y perpetuando la disfunción renal y cardiaca.
Intervenciones terapéuticas:
Sobrecarga de volumen:
La sobrecarga de líquidos es una de las principales consecuencias del SCR. Los diuréticos del asa se utilizan de manera casi universal para el alivio de la congestión y para mejorar los síntomas en la IC, y continúan siendo la piedra angular del tratamiento de la sobrecarga de volumen producido por el SCR.
A mayor congestión sistémica, mayor presión venosa central y en consecuencia aumento de la presión venosa renal que conlleva a la reducción del gradiente de presión existente a lo largo del glomérulo, que reduce el FG. El aumento de la presión intersticial renal puede conducir a una compresión tubular, hipoxia del parénquima y mayor reducción del FG, y la compresión extrínseca (por el aumento de la presión abdominal) de las venas renales y el parénquima, deteriora también la función renal.
Hasta no hace mucho tiempo, al momento de tratar a los pacientes con IC aguda (SCR tipo 1), la preservación de la función renal solía ser uno de los objetivo terapéuticos y un gran limitante de la dosis de diuréticos administrados. Es cada vez mayor la evidencia que indica que la IRA es consecuencia de la congestión venosa renal, y no de la depleción de volumen secundaria a la descongestión del paciente. El uso de menor dosis diurética está asociado a mayores eventos y peor pronóstico. El aumento aislado de la función renal, no indica por sí sola, peores resultados clínicos, en cambio es un indicador de mal pronóstico cuando está acompañada por congestión.
Y aunque los diuréticos de ASA son la primera línea de tratamiento de la sobrecarga hídrica en los pacientes con SCR, su utilización se encuentra frecuentemente limitada por la presencia de resistencia a los diuréticos en estos pacientes. Los mecanismos fisiopatológicos que explican principalmente este fenómeno incluyen: la reabsorción distal compensadora de sodio, la activación del SRAA y el aumento de la presión intra-abdominal por menor capacitación de la vasculatura esplácnica. Es importante resaltar que la resistencia a los diuréticos se asocia a hipotensión, disfunción renal oliguria y aumento de riesgo de re hospitalizaciones y muerte.
A pesar de que es un problema frecuente, continúa aun habiendo escasa evidencia para definir la mejor estrategia de tratamiento. Clásicamente se agregan diuréticos tiazídicos, aunque nueva evidencia indica la asociación podría aumentar eventos de hipokalemia, hiponatremia, falla renal y muerte. Por lo que aumentar la dosis de ASA, parece una alternativa más segura.
El agregado de antagonistas de los mineral corticoides, vasopresina, dopamina, y péptidos natriuréticos, podría ser otra posibilidad terapéutica, sin grandes resultados en estudios clínicos realizados en pacientes con IC y disfunción renal.
La diálisis y ultrafiltración son una opción terapéutica posible, en pacientes con mayor alteración de la función renal, que tampoco ha demostrado mayor beneficio.
En esencia, hay una clara falta de evidencia que ayude a guiar la sobrecarga de volumen en los pacientes con SCR. La mayoría de la información se extrapola de estudios realizados en pacientes con IC e IR. Y no en los diferentes escenarios del SCR.
Se han universalizado otras medidas como: la disminución del consumo de sodio en la dieta, la restricción de volumen, la suspensión de medicamente anti-hipertensivos en caso de hipotensión, la suspensión de AINES y otras medicaciones que pudiera empeorar el estado clínico de los pacientes con IC, se han sugerido aunque, por ausencia de evidencia y beneficio, la indicación no es clara.
Anemia, déficit de hierro y eritropoyetina:
Anemia, la resistencia y el déficit de Eritropoyetina (EPO) en los pacientes con IRC son posibles mecanismos fisiopatológicos de la disfunción cardiaca y renal.
Los efectos de EPO van más allá de la eritropoyesis. Múltiples órganos como el corazón y el riñón presentan receptores para ella, y participa de fenómenos tan variados como liberación de ON, la disminución de radicales libres, modulación de la inflamación y disminución de la activación del SRAA, todos mecanismos relacionados con el SCR.
La prevalencia de anemia en pacientes con IC crónica es alrededor del 50% y es aún más en pacientes con ICA descompensada. La presencia de la misma se asociada a mayor mortalidad. La terapia parenteral con hierro tiene evidencia, aunque conflictiva, y pareciera aumentar el beneficio en pacientes con IC crónica. En contraparte, el uso de la EPO no demostró beneficio y si potencial daño, por aumentar la viscosidad sanguínea. Es necesario profundizar la investigación en esta área para indicar conductas acertadas.
Enfermedad renal y cardiaca terminal:
En los pacientes con enfermedad renal terminal, el trasplante renal es una opción terapéutica viable. Posterior al trasplante renal, la clase funcional y sobrevida mejoran, así como las consecuencias deletéreas en el corazón generadas por la sobrecarga hídrica mejoran, tal como la hipertrofia ventricular, la FEY. En algunos casos la persistencia del SCR a pesar del trasplante se atribuye a la presencia de fistulas arterio-venosas (AV) de alto flujo que generan IC por hiperdinamia.
En contraposición, los sujetos con insuficiencia cardíaca terminal con indicación de trasplante, la IR es una contraindicación relativa, siendo más complejo su tratamiento. El trasplante bi-orgánico es una opción posible, aunque infrecuente.
El uso de dispositivos de asistencia ventricular avanzada es una opción aunque con escasa evidencia.
Pronóstico:
Al momento se carece de información pronóstica específica de cómo el SCR afecta la sobrevida de los pacientes con ambas afecciones. La evidencia actual extrapola la información obtenida por grandes registros y ensayos clínicos randomizados de pacientes con IC e IR concomitante, que arrojan que la falla renal es un marcador de mal pronóstico y peor sobrevida en los pacientes con insuficiencia cardíaca.
Conclusiones:
-El SCR describe una disfunción bidireccional concomitante del corazón y los riñones, en el cual un órgano inicia, perpetua y/o acelera el deterioro del otro.
-A pesar de la alta prevalencia y gran impacto deletéreo en los pacientes, el diagnóstico y tratamiento de los pacientes con SCR continua siendo dificultoso.
-Se necesita mayor investigación para entender los mecanismos fisiopatológicos generadores y perpetuadores del SCR, mejorar la exactitud diagnóstica, optimizar terapias existentes y descubrir nuevas estrategias de tratamiento efectivos.
-
– Ver link AQUI
Bibliografía
1-Ronco C, Haapio M, House AA, Anavekar N, Bellomo R. Cardiorenal Syndrome. Vol. 52, Journal of the American College of Cardiology. Elsevier USA; 2008. p. 1527–39.
2-McCullough PA, Kellum JA, Haase M, Müller C, Damman K, Murray PT, et al. Pathophysiology of the Cardiorenal Syndromes: Executive Summary from the Eleventh Consensus Conference of the Acute Dialysis Quality Initiative (ADQI). In 2013 [cited 2019 Dec 3]. p. 82–98. Available from: https://www.karger.com/Article/FullText/349966
1 comment










































1 Comment
Maria del Pilar Peña FiLio
enero 21, 2020, 8:33 pmBuenas tardes Muchas Gracias por mantenernos actualizados
REPLYFelicidades por su página.