El objetivo de este trabajo es proporcionar una guía práctica y resumida de las actualizaciones propuestas por la Sociedad Europea de Cardiología (a través de su guía 2016) para el diagnóstico y tratamiento de la insuficiencia cardíaca (IC). Los autores consideran que los cambios más importantes con respecto a la edición de 2012 hacen referencia
El objetivo de este trabajo es proporcionar una guía práctica y resumida de las actualizaciones propuestas por la Sociedad Europea de Cardiología (a través de su guía 2016) para el diagnóstico y tratamiento de la insuficiencia cardíaca (IC). Los autores consideran que los cambios más importantes con respecto a la edición de 2012 hacen referencia a 7 puntos, que son los que serán abordados en este escrito:
1- Recomendaciones claras sobre los criterios diagnósticos de la IC con fracción de eyección reducida (IC-FEr), la IC con fracción de eyección en rango medio (IC-FEm) y la IC con fracción de eyección conservada (IC-FEc)
La terminología más utilizada para describir a los tipos de IC continúa basándose en la determinación de la fracción de eyección (FE) del ventrículo izquierdo (FEVI). Así, se categoriza a los pacientes con FE conservada (IC-FEc), es decir ≥ 50% y a aquellos con FEVI reducida (IC-FEr), típicamente menor al 40%. Los pacientes con FEVI en la banda del 40-49% representan una «zona gris», que ahora se define como IC con FEVI en rango medio (IC-FEm).
El diagnóstico de la IC-FEc (que representan entre un 22-73 % de todos los pacientes con IC según las publicaciones) es más complejo que el diagnóstico de la IC-FEr, ya que los primeros generalmente no presentan dilatación del VI sino signos de aumento de las presiones de llenado (agrandamiento auricular o hipertrofia ventricular) y de disfunción diastólica. Es por eso que se unifican criterios para el diagnóstico de los pacientes con IC-FEc o IC-FEm:
Entonces para hablar de IC-FEc o IC-FEm debemos estar frente a un paciente con todo los siguiente:
- Presencia de síntomas o signos de IC.
- FE no reducida (definida como FEVI ≥ 50% o del 40-49% para la IC-FEm).
- Altas concentraciones de péptidos natriuréticos (PN): BNP > 35 pg/ml o NT-proBNP > 125 pg/ml, lo que representa una innovación respecto a guías anteriores.
- Al menos un dato objetivo de alteraciones cardiacas funcionales o estructurales subyacentes (agrandamiento auricular, hipertrofia ventricular, disfunción diastólica).
- En caso de incertidumbre, podría ser necesario realizar una prueba de estrés o determinar de manera invasiva un aumento de las presiones de llenado del VI para confirmar el diagnóstico.
Según los autores la identificación clara de estos 2 grupos (IC-FEc e IC-FEm) debería contribuir a la investigación de mejores estrategias de tratamiento. Sin embargo no existen novedades significativas en esta área, ya que los resultados de los ensayos clínicos publicados no encuentran beneficio pronóstico significativo en estos pacientes. Por lo tanto la orientación terapéutica debe ser dirigida a limitar el impacto de las comorbilidades, prevenir factores desencadenantes de la inestabilización clínica y emplear diuréticos para limitar la congestión.
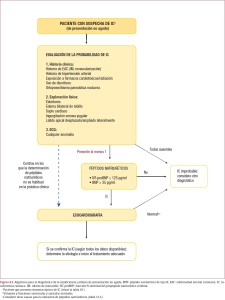
2- Nuevo algoritmo para el diagnóstico de la IC en presentación no aguda según la evaluación de la probabilidad de IC
En este nuevo algoritmo propuesto se hace hincapié en la concentración plasmática de péptidos natriuréticos (PN), proponiéndola como prueba diagnóstica inicial, especialmente en el contexto no agudo. Se resalta su valor predictivo negativo, excluyendo del diagnóstico de IC a aquellos pacientes con concentraciones de PN normales. Con este objetivo se aclaran los límites de corte en contexto no agudo (BNP: 35 pg/ml y NT-proBNP: 125 pg/ml) y agudo (BNP < 100 pg/ml y NT-proBNP < 300 pg/ml). Estos valores se aplican igualmente a la IC-FEr y la IC-FEc (a pesar de que como media, los valores son más bajos en la IC-FEc). Como salvedad se recuerda que una elevación de PN no basta por sí sola para el diagnóstico de IC ya que puede producirse por numerosas causas cardiovasculares y no cardiovasculares (fibrilación auricular, edad avanzada e insuficiencia renal). También es necesario remarcar que los títulos de PN pueden ser desproporcionadamente bajos en pacientes obesos.
El examen físico y la historia clínica conservan su lugar como valoración inicial. Los estudios complementarios básicos como el electrocardiograma (ECG) y el Ecocardiograma Doppler también mantienen su rol en este algoritmo: del primero se rescata su alta sensibilidad, que lo convierte en una herramienta útil para descartar el diagnóstico de IC cuando es completamente normal y del segundo su capacidad de establecer el diagnóstico y de diferenciar la IC-FEr de las otras formas, para así determinar el tratamiento más adecuado.
3- Recomendaciones para prevenir o retrasar la aparición de IC manifiesta o prevenir la muerte antes de la aparición de los síntomas
Este apartado va dirigido fundamentalmente a aquellas medidas destinadas al control de los factores de riesgo para prevenir o retrasar la aparición de IC y a la prevención de muerte súbita en pacientes asintomáticos.
Hipertensión arterial (HTA): se da relevancia al control de la HTA a través de determinados fármacos (diuréticos, inhibidores de la enzima convertidora de angiotensina [IECA], antagonistas del receptor de la angiotensina II [ARA-II], bloqueadores beta) ya que los mismos son efectivos en pacientes con o sin historia de infarto de miocardio. En cuanto al debate sobre los objetivos óptimos de tensión arterial (TA) para sujetos hipertensos no diabéticos, el reciente estudio SPRINT ha demostrado que tratar la HTA con un objetivo más bajo (TAS < 120 mmHg frente a < 140 mmHg) en pacientes hipertensos de edad ≥ 75 años o hipertensos de alto riesgo reduce el riesgo de enfermedad cardiovascular, muerte y hospitalización por IC, lo que obliga a replantear las metas más adecuadas.
Diabetes: se hace hincapié en el uso del tratamiento con empaglifozina (un inhibidor del cotransportador de sodio-glucosa de tipo 2) que recientemente ha demostrado reducir la mortalidad y las hospitalizaciones por IC en pacientes con diabetes mellitus tipo 2.
Enfermedad coronaria: se recomienda el uso de estatinas en paciente de alto riesgo o con antecedentes de enfermedad cardiovascular para reducir la tasa de complicaciones cardiovasculares, la mortalidad y la aparición de IC. En pacientes con enfermedad coronaria estable sin disfunción sistólica del VI o IC, se recomienda utilizar los IECA para prevenir o retrasar la aparición de IC y reducir la mortalidad cardiovascular. Asimismo, el aumento a dosis máximas toleradas de antagonistas del sistema renina-angiotensina puede mejorar la evolución, incluida la IC, de los pacientes coronarios con concentraciones plasmáticas de PN aumentadas. En caso de presencia de un infarto agudo de miocardio con elevación del segmento ST, tanto la revascularización temprana como la instauración precoz del tratamiento con IECA, bloqueadores beta o antagonistas de los receptores de mineralocorticoides (ARM) (especialmente cuando se asocia con disfunción sistólica del VI), reduce la tasa de hospitalizaciones por IC y la mortalidad.
Pacientes con FEVI reducida asintomáticos: independientemente de la etiología que genera la reducción en la FEVI, un IECA puede reducir el riesgo de IC que requiere hospitalización. Este beneficio no se ha demostrado con los bloqueadores beta o los ARM. Cuando el deterioro de la FEVI sea severo (< 30%) y de origen isquémico, se recomienda implantar un desfibrilador automático implantable (DAI) para prolongar la vida, al menos 40 días luego del sindrome coronario agudo.
4- Indicaciones para el uso del nuevo compuesto sacubitrilo/valsartán, el primero de la clase de inhibidores del receptor de la angiotensina y neprilisina (IRAN)
Los objetivos del tratamiento para los pacientes con IC no han sido modificados: mejorar el estado clínico, la capacidad funcional y la calidad de vida, prevenir las hospitalizaciones y reducir la mortalidad. En el caso de la IC-FEr, las piedras angulares continúan siendo los antagonistas neurohumorales (bloqueadores beta, IECA, ARM). La combinación inicial deberá ser la de betabloqueantes e IECA (de nuevo se relega a los ARA-II como alternativa a los IECA solo en casos de intolerancia). De persistir síntomas se adicionará un ARM. Esta recomendación se basa en los diseños de los ensayos clínicos con ARM, pero es cierto que en la práctica clínica la recomendación es de difícil aplicación, ya que suelen iniciarse desde el comienzo todos estos fármacos por su beneficio clínico y pronóstico. Estos 3 grupos de drogas (IECA/ARA-II, bloqueadores beta, ARM) deben ser llevados hasta la máxima dosis tolerada.
El nuevo compuesto LCZ696, que combina un ARA-II (valsartan) y un inhibidor de la neprilisina (sacubitrilo), se ha demostrado superior a un IECA (enalapril) para la reducción del riesgo de muerte y hospitalización por IC en un solo estudio con estrictos criterios de inclusión y exclusión. Se recomienda entonces el sacubitrilo-valsartan para sustituir a los IECA en pacientes que siguen sintomáticos pese a recibir el tratamiento médico óptimo (TMO) y que cumplen los criterios de dicho estudio (pacientes ambulatorios con IC-FEr sintomática, FEVI ≤ 35%, títulos aumentados de BNP o NT-proBNP, tasa de filtrado glomerular estimada ≥ 30 ml/min). Es necesario realizar un seguimiento de los pacientes en los que se utilice este nuevo compuesto ya que en el ensayo la hipotensión sintomática fue más frecuente en el grupo de sacubitrilo-valsartan. También es menester recordar que el riesgo de angioedema debe minimizarse suspendiendo el IECA al menos 36 horas antes de la administración de sacubitrilo-valsartan y nunca debe administrarse este compuesto en forma combinada con un IECA o ARA-II.
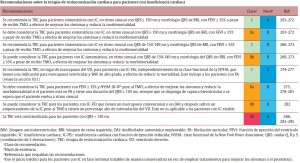
5- Modificación de las indicaciones para la terapia de resincronización cardiaca (TRC)
Cardiodesfibrilador implantable (DAI): en prevención secundaria su indicación se relaciona con la reducción de la mortalidad en los supervivientes a un paro cardiaco o aquellos que han sufrido arritmias ventriculares sintomáticas persistentes y tienen FEVI < 35% y ausencia de otras enfermedades que puedan causar la muerte en un plazo de 1 año.
En prevención primaria, el DAI reduce la tasa de muerte súbita por arritmias de los pacientes con IC-FEr. Este beneficio es mayor en paciente con IC de origen isquémico (siempre que se implante al menos 40 días tras un infarto agudo de miocardio) y en aquellos con IC leve (NYHA II), ya que en pacientes con IC moderada o grave, la reducción de la tasa de muerte súbita puede compensarse por el aumento de muertes debido al empeoramiento de la IC. Por este motivo la guía recomienda su uso como prevención primaria en pacientes con IC-FEr (FE < 35%) a pesar del TMO, que estén en clase funcional II-III con un mayor nivel de evidencia en pacientes con cardiopatía isquémica frente a los no isquémicos. La aparición de los resultados del estudio DANISH, posterior a la publicación de la guía podría implicar un cambio en la indicación de DAI para pacientes con miocardiopatía no isquémica al no hallar beneficio del implante en estos casos.
Los pacientes con indicación de DAI y duración del complejo QRS ≥ 130 mseg, deben ser valorados para tratamiento mediante desfibrilador con TRC (CRT-D). No se recomienda el tratamiento con DAI para pacientes en NYHA IV refractarios a tratamiento médico que tengan una esperanza de vida corta y muchas probabilidades de morir por fallo de bomba, como así también pacientes con otras comorbilidades graves que tienen pocas probabilidades de vivir más de 1 año. Importante también es resaltar que al alcanzar el generador del DAI el final de su vida útil no debe ser reemplazado automáticamente, sino que debe valorarse nuevamente el riesgo arrítmico y global del paciente. Se nombra en la guía la posibilidad de usar el ¨chaleco desfibrilador¨ (un DAI portátil externo) para pacientes con IC y alto riesgo de muerte súbita pero que no son candidatos a implante de DAI (FEVI reducida tras daño miocárdico agudo hasta que se recupere la función del VI, pacientes pre-trasplante)
Terapia de resincronización cardíaca (TRC): Las recomendaciones de la TRC se han actualizado para los pacientes con FEVI ≤ 35% que persistan sintomáticos a pesar del TMO, en ritmo sinusal, sin diferenciar la clase funcional de la NYHA en la que se encuentren (II-IV). Los principales criterios para su indicación pasan por la duración del complejo QRS y la morfología del mismo. El mayor grado de recomendación es para los pacientes con QRS > a 150 mseg y morfología de bloqueo completo de rama izquierda (BCRI), mientras que en menor grado debe considerarse en pacientes con QRS entre 130-150 mseg y morfología distinta al BCRI. En pacientes con QRS < 130 mseg no se recomienda su uso, más allá de la utilización de métodos de imágenes que pudieran demostrar asincronía. Resulta pertinente mencionar aquellas características del paciente que predicen una mejor respuesta a esta terapéutica: el grado de remodelado, la etiología no isquémica y el sexo femenino. En pacientes con FEVI reducida que requieran estimulación eléctrica del VD (a causa de bradiarritmias por ejemplo), ésta puede exacerbar la disincronía cardiaca por lo que se recomienda la TRC más que la estimulación aislada del VD, independientemente de la clase funcional. Con relación a los pacientes con FA la evidencia es controversial, pero está a favor del uso de TRC siempre que se logre una captura biventricular elevada.
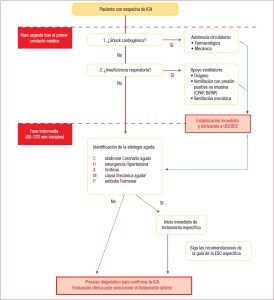
6- El concepto de instauración de tratamiento temprana y simultánea a la realización de pruebas relevantes en la IC aguda (ICA), según la estrategia de «tiempo transcurrido hasta tratamiento» que ya se aplica en los síndromes coronarios agudos (SCA)
La ICA, definida como la aparición rápida o el empeoramiento de los síntomas o signos de IC se puede presentar como primera manifestación (de novo) o, más frecuentemente, como consecuencia de una descompensación aguda de la IC crónica. Puede estar causada por una disfunción cardiaca primaria o precipitada por factores extrínsecos.
En los pacientes con cuadros agudos, debido a la alta mortalidad, el inicio precoz del tratamiento adecuado, así como las pruebas diagnósticas necesarias son de suma importancia. Para ello, ante la sospecha clínica de ICA, deberá en primer lugar estabilizarse al paciente, ya sea con asistencia circulatoria (farmacológica o mecánica) en caso de shock cardiogénico o apoyo ventilatorio en casos de insuficiencia respiratoria.
El proceso diagnóstico deberá iniciarse en paralelo al tratamiento en estos pacientes. En ese sentido, el aporte de examenes básicos (pruebas de laboratorio, radiografía de tórax, ECG) es indudable, pero se hace foco en la utilidad de los PN gracias a su alta sensibilidad y a la capacidad de discernir entre la IC y otras causas no cardiacas de disnea aguda (al ser normales el diagnóstico de ICA es improbable). La determinación de troponinas es útil para la detección de un síndrome coronario agudo como causa descompensante de la ICA, sin embargo, en la mayoría de los cuadros agudos estos valores pueden estar elevados por daño o lesión miocárdica aún en ausencia de isquemia. El ecocardiograma se recomienda en las primeras 48 horas salvo en casos de inestabilidad hemodinámica o sospecha de causas potencialmente letales, en cuyo caso debe realizarse inmediatamente.
Realizado el diagnóstico y el tratamiento inicial en forma precoz, el siguiente paso propuesto consiste en identificar los factores desencadenantes o causas principales que producen la descompensación, que también se deben tratar urgentemente para evitar un mayor deterioro. Ellos incluyen (se recomienda utilizar la regla nemotécnica CHAMP) : SCA (la coexistencia de SCA e ICA obliga a la revascularización de urgencia en menos de 2 horas desde el ingreso), emergencia hipertensiva (tratamiento con vasodilatadores endovenosos y diuréticos de asa), arritmias rápidas o bradicardia/alteraciones del ritmo graves (requerirán cardioversión eléctrica o marcapaseo transitorio), causa mecánica aguda subyacente a la ICA (el ecocardiograma asume un rol vital y el tratamiento requiere normalmente apoyo circulatorio con intervención quirúrgica o percutánea) o embolia pulmonar aguda (anticoagulación o fibrinólisis de acuerdo al caso).
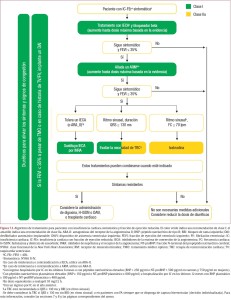
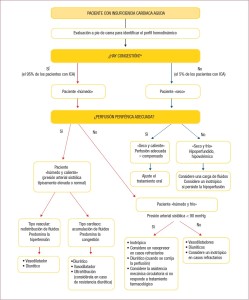
7- Un nuevo algoritmo para una estrategia combinada de diagnóstico y tratamiento de la ICA según la presencia o ausencia de congestión e hipoperfusión.
La guía amplía el apartado dedicado a la ICA respecto a la edición anterior al proponer un algoritmo diagnóstico/terapéutico basado en la clasificación de Nohria, la cual se basa en la exploración física al pie de la cama para detectar síntomas/signos clínicos de congestión («húmeda» frente a «seca») o hipoperfusión periférica («fría» frente a «caliente»). La combinación de estas opciones permite identificar 4 grupos de pacientes para guiar la fase inicial del tratamiento y aportar información pronóstica.
COMENTARIOS FINALES
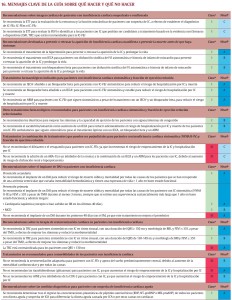
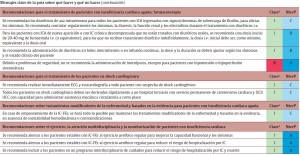
Sin duda la presente guía constituye un documento importante para la práctica médica habitual al presentar de forma clara recomendaciones (en su mayor parte con un alto nivel de evidencia) útiles con respecto al manejo de estos pacientes, al uso de nuevos fármacos y dispositivos. Sin embargo, siguen existiendo ciertas falencias en la evidencia, más que nada en lo que respecta al tratamiento de pacientes con insuficiencia cardíaca con FE no reducida que se espera tengan un avance en ediciones futuras. De particular importancia en el quehacer médico cotidiano resultan mensajes contundentes como los comentarios finales del documento en los que se aconseja «qué hacer y qué no hacer» con los pacientes con IC, resumiendo aquellas recomendaciones clase I y III. Es por ese motivo que estos consejos se adjuntan a continuación como cierre final.
- Descargar PDF «Guia 2016 ESC ICC»













































2 Comments
Gabriel Carranza
marzo 4, 2018, 11:29 pmMuy buen resumen, gracias por el aporte.
REPLYCamila M
noviembre 26, 2018, 1:43 amExcelente resumen, muchas gracias…
REPLY