Como es bien conocido a partir de los registros de Framingham y otros, la fibrilación auricular (FA) es la arritmia mas frecuente y se calcula que una de cada cuatro personas padecerá a lo largo de su vida de un episodio de fibrilación auricular de distinta duración y compromiso clínico[i]–[ii]. Un modo extremadamente simple pero
Como es bien conocido a partir de los registros de Framingham y otros, la fibrilación auricular (FA) es la arritmia mas frecuente y se calcula que una de cada cuatro personas padecerá a lo largo de su vida de un episodio de fibrilación auricular de distinta duración y compromiso clínico[i]–[ii].
Un modo extremadamente simple pero práctica consiste en dividir la fibrilación auricular -particularmente autolimitada, esporádica o paroxística, aunque en algunos casos también persistente- en dos grandes grupos: aquellas presentes en corazón sano y las que se manifiestan en corazón enfermo. Dentro de la primera categoría, salvo FA primarias originadas en mutaciones genéticas, la mayoría tienen origen en alteraciones funcionales en que el sistema nervioso autónomo (SNA) juega un papel fundamental. En este caso se considera a la FA una alteración tal, que en alguna oportunidad se debatió acerca si realmente se trata de una enfermedad[iii]. A pesar de ello, esta arritmia sin cardiopatía puede determinar significativos cambios en la calidad de vida, a moderado o largo plazo alteraciones en la función auricular e incluso ventricular, y hasta impacto psicosocial de magnitud, lo que justifica su tratamiento.
¿Cuál es la razón por la que se generan estos episodios -muchas veces asintomáticos- en corazón aparentemente sano o con mínimas alteraciones? No cabe duda que el SNA juega un papel fundamental tanto en su precipitación, mantenimiento como en su resolución.
Antes de ingresar en los mecanismos que generan FA a pesar de no presentar cardiopatía alguna, se debe resignificar esta arritmia como de origen funcional y autonómica. La FA paroxística autolimitada sin cardiopatía, es mucho más frecuente que la que suele ingresar en los registros como FA solitaria o “lone atrial fibrillation”, llegando en algunos casos al 30%[iv] de los portadores de esta arritmia. Suele ser urbana, relacionada a situaciones de stress, en muchos casos relacionado a reflujo gastroesofágico, gastritis y esofagitis[v], en otros con apneas del sueño, ingesta de alcohol[vi], etc. todos ellos gatillos desencadenantes predominantemente vagales, en una situación predisponente física y psíquica. También es vagal la precipitación frecuente de los episodios de FA sin cardiopatía en horarios vespertinos o de madrugada[vii]. En todos los casos es necesario un gatillo que necesariamente comienza con extrasístoles auriculares aisladas y en salvas. Entender en que situaciones se generan estas salvas permiten reducir su incidencia y en consecuencia la FA sin cardiopatía -y en muchos casos con- es prevenible con cambios en el estilo de vida lo que incluye la actividad física y la dieta. El cambio de mentalidad del médico y del paciente frente a la FA, tal como se observa en los últimos años, es una buena noticia. Se están conociendo respuestas a preguntas básicas relacionadas a FA lo que hace que cada vez estemos más cerca de su prevención.
Se conoce desde hace muchos años[viii] el papel del SNA, y se sabe que las salvas de extrasístoles remodelan las aurículas que terminan formando rotores que finalmente desencadenan la FA. Esto se publica desde 1962[ix]. Cerebro, pulmones y el sistema inmunológico están conectados e interactúan para desencadenar e incluso hacer persistente una FA autolimitada o paroxística.
El tratamiento de la FA y su prevención no son fáciles y por esa razón conocer qué papel juega la conexión cerebro-corazón -es decir el SNA- es fundamental. La relación entre la inervación cardíaca del sistema nervioso autónomo y la FA se profundizó el siglo pasado, cuando estimulando los troncos del SNA vago/simpáticos se observó que acortan en forma heterogénea los períodos refractarios de las células auriculares generando dispersión de la refractariedad.
Las venas pulmonares son susceptibles de generar arritmias por estimulación vagal. La acetilcolina induce taquicardias reentrantes en estas venas, una de las bases de producción de FA por sobrecarga intracelular de Ca++ y el consiguiente acortamiento del período refractario.
En ese caso la introducción de extrasístoles permite inducir al caos (desorden del automatismo y excitabilidad) que representa la FA. A principios de este siglo se investigó otro aspecto de la inervación autonómica del corazón a partir de plexos ganglionares en el corazón mismo y grandes vasos[x]. A ese se lo llamó Sistema Nervioso Autónomo Intrínseco Cardíaco, local, distinto a la conexión cerebro y médula que inerva al corazón, llamado de esta manera extrínseco. El sistema intrínseco de plexos ganglionares está ubicado al margen de las venas pulmonares, actúa como repetidor de estímulos del sistema extrínseco vago/simpático, pero puede actuar de forma independiente modulando funciones cardíacas como automatismo, excitabilidad y conducción. La estimulación, sea eléctrica o química a través de neurotransmisores inducen los disparos focales de las venas pulmonares. La ablación de los plexos ganglionares relacionados a las venas pulmonares disminuye la inducibilidad de FA[xi]. La experiencia clínica y de laboratorio demuestra que esta forma de FA, secundaria a variaciones del tono autonómico no responde al tratamiento con antiarrítmicos clase III o IC[xii].
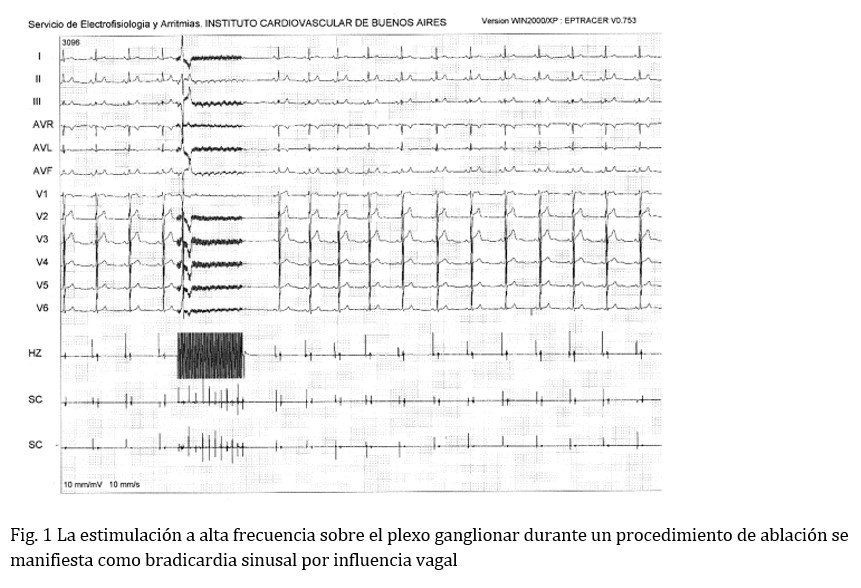
Los plexos ganglionares vecinos a las venas pulmonares se identifican con la aplicación de estímulos de alta frecuencia a estos grupos de nervios[xiii] (Fig 1)
Otra prueba del papel del equilibrio vago/simpático en la persistencia de FA, es la identificación mediante el análisis espectral de los sitios de alta frecuencia, representativos del tono vagal incrementado[1] En pacientes con formas persistentes de FA, la respuesta fue una disminución marcada de la respuesta ventricular (≥50%) durante la FA. Los resultados de la ablación de estos plexos son variables respecto de la recurrencia de la FA, en algunos casos muy alta (96%) pero baja en otros estudios, como resultado de ablaciones parciales[2]. Se sabe que la ablación parcial del plexo ganglionar puede incluso aumentar la incidencia de FA al exacerbar la heterogeneidad de la refractariedad a través de las aurículas promoviendo FA macro-reentrante[3]. Varios estudios se realizaron combinando ambas técnicas de aislamiento de venas pulmonares y de los plexos ganglionares[4], incluso con técnicas modernas de crioablación[5]. Un estudio aleatorizado relativamente reciente[6] muestra que los resultados son significativamente mejores que sólo el aislamiento de las venas pulmonares, en un seguimiento de 12 meses. Funcionalmente, los ganglios mencionados muestran una mayor sensibilidad a los neurotransmisores colinérgicos y adrenérgicos que los tejidos auriculares adyacentes.
Es necesario comprender tanto en la clínica como desde el punto de vista electrofisiológico, que se deben tener en cuenta los mecanismos tanto autonómicos como miocárdicos para explicar el desencadenamiento así como la persistencia de la FA.
La experiencia muestra que la incidencia de episodios de FA en corazón aparentemente sano es mayor entre los 50 y 70 años de edad. Estudiadas las respuestas cardiovasculares a las influencias autonómicas en mujeres y hombres sanos que incluían grupos de 25, 45 y 60-80 años sugieren que habría una atenuación moderada de las respuestas cardiovasculares autonómicas hasta aproximadamente los 60 años, después de lo cual se produce un declive más rápido[7]. Otra investigación mostró que la estimulación vago/simpática del tronco podría abolir la activación neural dentro del plexo ganglionar anterior derecho vecino a la vena pulmonar superior derecha[8]. El paso de FA paroxística a persistente, se explica entre otros, debido al hecho de que a medida que aumenta la carga de FA, la actividad de los plexos ganglionares aumenta dando como resultado una liberación excesiva de neurotransmisores muscarínicos y adrenérgicos localmente y a través de sus campos axonales a grupos más pequeños de ganglios que comprenden la red neuronal interconectada que cubre las aurículas. La liberación excesiva de neurotransmisores localmente aporta otro factor que explica el efecto «FA engendra FA»[9]
Cabe mencionar que la ablación de los plexos ganglionares como un procedimiento complementario para el aislamiento de la vena pulmonar todavía no alcanza el mismo grado de éxito que el logrado mediante procedimientos de ablación con catéter dirigidos a pacientes con vías anómalas, reentrada intranodal o aleteo auricular. Obviamente, la FA es una arritmia más compleja en la que intervienen más de un mecanismo o una coexistencia de mecanismos.
Una visión global en el tratamiento y la prevención de la FA en pacientes en corazón aparentemente normal implica en primer lugar, que el médico entienda de que se trata en estos casos de un disturbio funcional en donde intervienen la personalidad, stress e incluso factores socio económicos[10], con un importante contenido autonómico, lo que permite que el paciente sea contenido, comprenda que no es mortal ni va a generar un colapso salvo circunstancias puntuales y comorbilidades específicas. El médico debe conversar con el paciente, comprenderlo, explicar su situación, y hacerle entender que no es una amenaza para su vida[11]. Incluso puede no tratarse, dado que en más del 90% de los casos la reversión en estos casos es espontánea. Se debe explicar que el riesgo de accidente cerebrovascular es mínimo si no tiene cardiopatía o ciertas morbilidades que conocemos como CHA2DS2-VASc Score. La conducta que no comienza con fármacos o intervenciones sino con lo que desde siempre se ha llamado régimen higiénico/dietético[12]. La rigurosa aplicación de las guías internacionales de tratamiento de la FA muestra este camino.[13]–[14]
REFERENCIAS
[1] P Sanders, O Berenfeld, M Hocini, P Jaïs, R Vaidyanathan, Li-Fern Hsu, S Garrigue, Y Takahashi, M Rotter, F Sacher, C Scavée, R Ploutz-Snyder, J Jalife, M Haïssaguerre, Spectral Analysis Identifies Sites of High-Frequency Activity Maintaining Atrial Fibrillation in Humans Circulation. 2005;112:789-797
[2] M. Scanavacca, C. F. Pisani, D. Hachul et al., “Selective atrial vagal denervation guided by evoked vagal reflex to treat patients with paroxysmal atrial fibrillation,” Circulation, 2006 114:876–885,.
[3] E. Mikhaylov, A. Kanidieva, N. Sviridova et al., “Outcome of anatomic ganglionated plexi ablation to treat paroxysmal atrial fibrillation: a 3-year follow-up study,” Europace, 2011 13: 362–370,.
[4] Jhuo SJ1, Lo LW2, Chang SL2, Lin YJ2, Chung FP3, Chiou CW2, Chen SA4. Periesophageal vagal plexus injury is a favorable outcome predictor after catheter ablation of atrial fibrillation. Heart Rhythm. 2016 Sep;13(9):1786-93
[5] Yorgun H, Aytemir K, Canpolat U, Şahiner L, Kaya EB, Oto A. Additional benefit of cryoballoon-based atrial fibrillation ablation beyond pulmonary vein isolation: modification of ganglionated plexi. Europace. 2014 May;16(5):645-51
[6] D. G. Katritsis, E. Giazitzoglou, T. Zografos, E. Pokushalov, S. S. Po, and A. J. Camm, “Rapid pulmonary vein isolation combined with autonomic ganglia modification: a randomized study,” Heart Rhythm, 2011 8: 672–678,.
[7] L. Kaijser and C. Sachs, “Autonomic cardiovascular responses in old age,” Clinical Physiology, 1985 5: 347–357,.
[8] Y. Zhang, B. J. Scherlag, Z. Lu et al., “Comparison of atrial fibrillation inducibility by electrical stimulation of either the extrinsic or the intrinsic autonomic nervous systems,” Journal of Interventional Cardiac Electrophysiology, 2009 24:5–10,.
[9] Y. Hou, B. J. Scherlag, J. Lin et al., “Interactive atrial neural network: determining the connections between ganglionated plexi,” Heart Rhythm, 2007 4 56–63,.
[10] A VMattioli, S Bonatti, M Zennaro, G Mattioli The relationship between personality, socio-economic factors, acute life stress and the development, spontaneous conversion and recurrences of acute lone atrial fibrillation Europace. 2005 7 (3): 211-20
[11] Giniger A Fibrilación auricular esporádica o paroxística y corazón sano: la industrialización de la prevención y el tratamiento Rev Arg de Cardiol 2003 71:307-8,
[12] Giniger A La fibrilación auricular recurrente benigna del adulto lone atrial fibrillation es una enfermedad ? Rev Arg de Cardiol 2007 75:2-5,
[13] European Heart Rhythm Association (EHRA) position paper on arrhythmia management and device therapies in endocrine disorders, endorsed by Asia Pacific Heart Rhythm Society (APHRS) and Latin American Heart Rhythm Society (LAHRS). Europace. 2018 Mar 16
[14] Management of patients with atrial fibrillation (compilation of 2006 ACCF/AHA/ESC and 2011 ACCF/AHA/HRS recommendations): a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2013 May 7;61(18):1935-44
1 comment







































1 Comment
Carlos Benjamin Alvarez
abril 17, 2023, 9:25 amExcelente articulo general de la intervencion del SNAen la genesis de la FA,en corazones estructuralmente normales
REPLY