El trombo intraventricular (TIV) es una entidad que conlleva un riesgo significativo de accidente cerebrovascular (ACV) o embolia sistémica. En series antiguas, su prevalencia era mayor al 30% en pacientes post infarto agudo de miocardio (IAM). Su incidencia disminuyó en las últimas décadas debido a dos factores principales, la angioplastia coronaria (ATC) y la utilización
El trombo intraventricular (TIV) es una entidad que conlleva un riesgo significativo de accidente cerebrovascular (ACV) o embolia sistémica. En series antiguas, su prevalencia era mayor al 30% en pacientes post infarto agudo de miocardio (IAM). Su incidencia disminuyó en las últimas décadas debido a dos factores principales, la angioplastia coronaria (ATC) y la utilización de doble antiagregación plaquetaria (DAPT), aunque su prevalencia se reporta entre un 3-9% de los infartos transmurales.
Esta entidad tiene algunos desafíos clínicos, principalmente relacionados al tratamiento anticoagulante, sobre todo porque estos pacientes necesitan tratamiento con DAPT concomitante.
Si bien hay muchos datos sobre la prevalencia de TIV en pacientes con miocardiopatías dilatadas isquémicas, poco se sabe sobre la prevalencia en la etiología no isquémica.
Los mecanismos fisiopatológicos de la TIV son múltiples, pero se reconocen la disfunción ventricular izquierda y su dilatación, y el estado protrombótico asociado a la insuficiencia cardíaca congestiva.
El tratamiento anticoagulante aprobado para la prevención de eventos tromboembólicos en este contexto son los antagonistas de la vitamina K (AVK). Existen datos limitados de la utilización “off label” de anticoagulantes orales directos (DOAC), y se requiere más evidencia para justificar su uso en la práctica clínica.
Esta revisión analiza la prevalencia, mecanismos fisiopatológicos y las opciones terapéuticas disponibles sobre el TIV1.
Prevalencia
Post-Infarto agudo de miocardio
En la era pre ATC y pre trombolítica, la prevalencia global del TIV post-IAM se reportó entre 17-24%, siendo mayor en aquellos de localización anterior 28-34%.
En la era post-ATC, existe una gran dispersión de la misma, que va desde 0,4% en 157.891 pacientes con IAM anterior evaluador por ecocardiograma, hasta el más alto de 26% en 100 pacientes con IAM de la misma localización. Esta diferencia radica en la diferente selección de pacientes, técnicas diagnósticas y tratamiento antitrombóticos utilizados.
En estudios que utilizaron resonancia magnética (RMC), considerado el gold-standard como estudio diagnóstico, reportaron una prevalencia global del 8%, con un rango entre 7-26% en infartos de cara anterior.
Cardiopatía no isquémica
Los datos son limitados sobre epidemiología de la TIV en pacientes sin cardiopatía isquémica. En pacientes con miocardiopatía dilatada, la TIV puede desarrollarse como complicación debido a la éstasis sanguínea en aquellos con dilatación severa del ventrículo izquierdo (VI).
A diferencia de los adultos, en pacientes pediátricos, la miocardiopatía dilatada conlleva a un riesgo elevado de TIV, con una prevalencia entre 6-53%.
En el curso de una miocardiopatía hipertrófica, la disfunción sistólica apical con aneurisma puede complicarse con TIV.
Estudios observacionales reportan un rango amplio de incidencia en pacientes en fase aguda de Takotsubo, siendo la más alta de 14% en presencia de baloneamiento apical y elevación de troponina I. El registro Internacional de Takotsubo reportó una prevalencia del 3.3%.
Los trombos intracardíacos son frecuentes en pacientes con amiloidosis. La serie más grande publicada por DaLi Feng y cols (159 pacientes con amioloidosis cardíaca) reportó un 27% (42p) de trombosis intracardíaca, aunque un 88% localizado en la orejuela auricular.
Otras miocardiopatías con baja prevalencia reportada son el síndrome hipereosinofílico y la enfermedad de Behcet.
Predictores clínicos y factores de riesgo
La escara apical y la disfunción sistólica VI son dos factores de riesgo asociados a TIV post IAM, con amplia evidencia.
La disfunción sistólica VI es uno de los predictores independientes más fuertes para la formación de TIV.
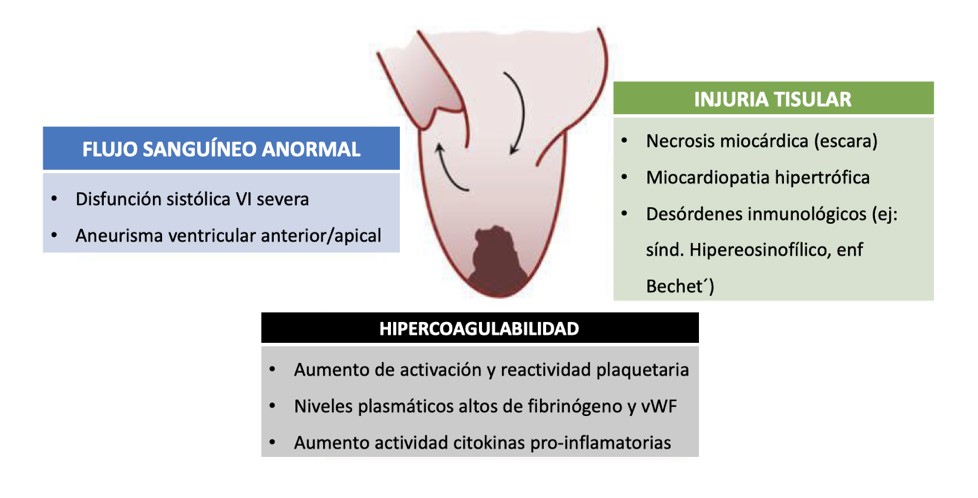
La tríada de Virchow está presente como característica principal en la miocardiopatía dilatada post-infarto: flujo sanguíneo anormal, hipercoagulabilidad e injuria tisular de la pared (figura 1)
Figura 1: tríada de Virchow
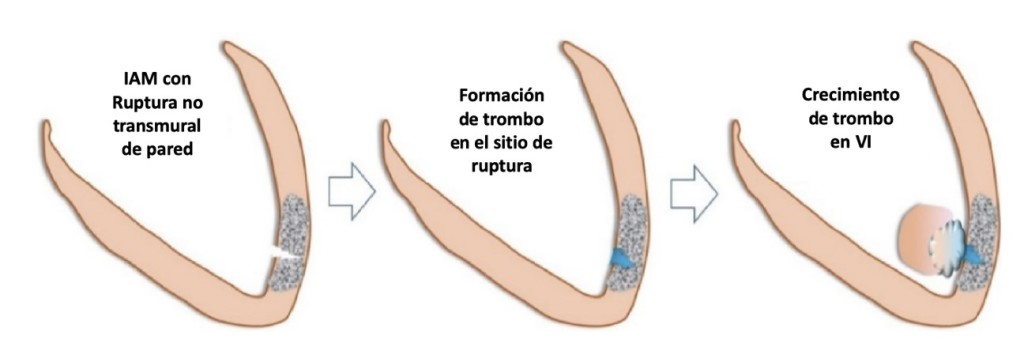
Recientemente, Ma Shan y cols. proponen una hipótesis fisiopatológica distinta. La mayoría de los TIV post- IAM se presentan en los primeros días posteriores al evento coronario, en éstos, los autores sugieren que la TIV se relaciona con la ruptura incompleta de pared ventricular (figura 2). Esta afirmación está basada en reportes de casos donde aquellos pacientes en los que se encontró TIV en los primeros días post-IAM, presentaron alta mortalidad por ruptura VI; por otro lado, estudios animales experimentales en ratas y ratones han reproducido estos hallazgos. 2
Figura 2: Ruptura incompleta de pared ventricular izquierda2
Otros estudios han evaluado el impacto de la insuficiencia mitral (IM) en la formación de trombos, algunos asociándolos a un efecto protector como consecuencia de la disminución en la éstasis sanguínea, y otros autores, como Ascione y cols. asociaron la IM severa con alta incidencia de eventos tromboembólicos y TIV, aunque estos resultados, pueden deberse a la extensión de los trastornos de motilidad asociados a la TIV y la IM, actuando como un confundidor, de hecho, en el análisis multivariado la inclusión de la IM no modificó los resultados.
Hay un nexo entre la insuficiencia cardíaca (IC) congestiva y un estado protrombótico. Existe un tiempo de sobrevida plaquetario reducido, un volumen plaquetario aumentado y una mayor activación de las mismas en el contexto de la IC congestiva. Pacientes con IC con o sin fracción de eyección reducida presentan altos niveles de fibrinógeno circulante, dímero D y factor von Willebrand (vWF), reforzando la asociación entre IC e hipercoagulabilidad. Aquellos pacientes con aneurisma apical o anterior tienen niveles plasmáticos de fibrinógeno y vWF elevados, en comparación con aquellos de la misma edad, con enfermedad coronaria y ausencia de aneurisma VI.
Los estados proinflamatorios también pueden inducir el aumento en los niveles de vWF y fibrinógeno, y así contribuir en las complicaciones trombóticas de la IC congestiva.
Herramientas diagnósticas
El test inicial para la detección de TIV es el ecocardiograma transtorácico (ETT) ya que es utilizado de rutina en pacientes con IAM para evaluar su función sistólica y estructura, además de descartar complicaciones mecánicas. El TIV se aprecia como una masa hiperecogénica con bordes bien definidos y separados del endocardio, contiguo a un trastorno de la motilidad segmentaria, aquinesia, hopokinesia severa o aneurisma. El trombo puede observarse como una masa protuberante (sésil o pedunculada) adherida al VI mientras que el trombo mural son masas planas. Las principales desventajas del ETT en la detección del TIV es la visualización del ápex verdadero, la presencia de trombo mural pequeño y una ventana ultrasónica subóptima. Aunque la literatura reporta una precisión diagnóstica del 90% comparada con la RMC, es muy dependiente de la calidad de imagen.
El ecocardiograma transesofágico (ETE) no es un buen estudio para TIV ya que no permite una adecuada visualización del ápex.
El contraste mejora la definición de los bordes endocárdicos y la calidad de imagen para la detección de TIV en pacientes con IAM anterior. A pesar de ello, un tercio de los TIV diagnosticados por RMC no son detectados a pesar de la utlización de contraste.
La RMC es considerada la técnica gold standard para evaluar la presencia, tamaño y localización de TIV. Se detecta como un defecto de relleno intraventricular de baja señal adherido a un área de realce VI (escara).
Aún no podemos determinar el tiempo evolutivo de los trombos con las técnicas de imágenes actuales.
Riesgo de embolia
El TIV se asocia con aumento en el riesgo de embolia, principalmente durante las 2 primeras semanas post- IAM. Un estudio de cohorte reciente, midió la incidencia de embolia sistémica de pacientes con TIV durante un promedio de 3 años, y encontró una tasa anual combinada de ACV, accidente isquémico transitorio (AIT) y embolia sistémica de 3.7%, 4 veces más alto que el grupo sin TIV.
La movilidad y protrusión del trombo son los principales factores de riesgo de embolias.
Opciones terapéuticas
Guías internacionales
Las guías internacionales recomiendan de manera unánime el tratamiento anticoagulante en pacientes con TIV.
Las sociedades más importantes como el American College of Chest Physicians (ACCP), American Heart Association (AHA) y European Society of Cardiology (ESC) sugieren en sus guías la anticoagulación con antagonistas de la vitamina K (AVK) como terapia de primera línea.
Un metanálisis de 11 estudios observacionales probaron que la anticoagulación con AVK disminuyó efectivamente el riesgo de formación de TIV y embolización. Aunque la anticoagulación con AVK es probablemente tan efectiva y más práctica que la anticoagulación con heparina, no existen ensayos aleatorizados que hayan comparado de manera prospectiva la terapia con AVK con la terapia parenteral.
Hay consenso en la anticoagulación con AVK tan pronto como se realiza el diagnóstico de TIV y la anticoagulación parenteral se suspenderá una vez alcanzado el rango terapéutico (INR 2-3). Todas las guías recomiendan un ETT a los 3 meses.
La anticoagulación debe discontinuarse tan pronto como se establezca la resolución del trombo: habitualmente se requiere de 3 meses.
En caso de persistencia del TIV, se recomienda continuar con anticoagulación y reevaluación con nuevo método de imagen. (Figura 3)
Un punto a tener en cuenta es la utilización de triple terapia antitrombótica, que consta en doble terpia antiagregante (DAPT) y AVK. La triple terapia aumenta el riesgo de sangrado, evento adverso demostrado en numerosos ensayos clínicos aleatorizados de gran escala en pacientes con fibrilación auricular (FA). Es por ello, que las guías ESC 2017 de DAPT y 2019 en síndrome coronarios crónicos plantean que la duración de la triple terapia antitrombótica debe minimizarse en función del riesgo de sangrado / isquemia, siendo mayor a 1 mes cuando los pacientes presentan un riesgo de trombosis intrastent que supera el de sangrado.
Anticoagulantes orales directos (DOAC)
No hay suficientes datos disponibles sobre el uso de DOAC para reemplazar los AVK en pacientes con TIV. Los DOAC se investigaron en dos revisiones de reporte de casos de 36 y 41 pacientes. También hay, unos pocos estudios retrospectivos, siendo un registro monocéntrico retrospectivo el primero en publicarse, que evaluó 52 casos de TIV tratados con DOACs. Todos estos estudios reportaron en el seguimiento, una resolución del trombo mayor al 80%. Estos ensayos tienen la limitación de los sesgos de publicación que poseen los reportes de casos. Los últimos datos provienen de 2 análisis retrospectivos. El grupo del estudio ACTION que colectó 159 pacientes con TIV, y aunque el estudio no fue diseñado ni tuvo el poder para comparar de manera directa DOAC con AVK, sugirió una tasa similar de regresión del trombo con ambas terapias anticoagulantes. Con otros resultados, el ensayo multicéntrico de cohorte retrospectivo de 514 pacientes seguidos por 351 días, encontró que el tratamiento con DOACs se asoció a mayor riesgo de ACV isquémico y embolia sistémica que AVK.
Estos resultados deben considerarse exploratorios, ya que se necesitan ensayos clínicos aleatorizados.
Inhibidores de los receptores P2Y12
La introducción de inhibidores P2Y12 potentes en la práctica clínica puede haber contribuido en la reducción de la incidencia de TIV post-IAM, como sugieren análisis retrospectivos que compararon ticagrelor y clopidogrel. Aunque es biológicamente plausible, no hay ensayos en la literatura que confirmen la protección del DAPT contra la formación de TIV, por lo tanto, no debe considerarse como una terapia sustituta de la anticoagulación.
Tratamiento quirúrgico para el TIV
La remoción quirúrgica del trombo VI es una opción para pacientes con alto riesgo embólico, por ejemplo, pacientes que se someterán a ECMO. Mientras que la remoción quirúrgica podría disminuir la incidencia de tromboembolismo más efectivamente que la terapia anticoagulante, el riesgo no necesariamente pesa más el beneficio, y no está recomendada la cirugía cardíaca cuando la indicación sólo se limita a la TIV.
Algoritmo diagnóstico y terapéutico
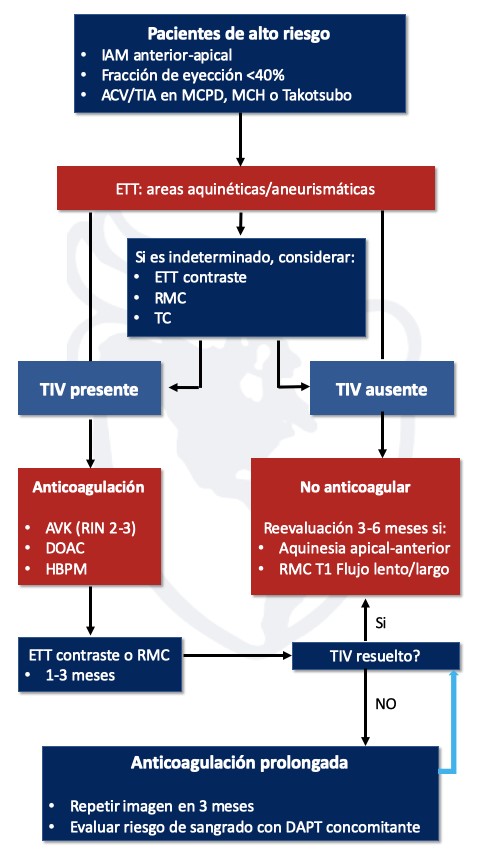
En este algoritmo (Figura 3), los autores recomiendan el ETT como método diagnóstico de primera línea. En caso de resultado indeterminado o persistencia de alta sospecha de TIV, se recomienda un segundo test como el ETT con contraste, RMC o tomografía computada. En casos no concluyentes o de alto riesgo de sangrado, se prefiere una estrategia de imágenes seriadas. En casos de intolerancia a AVK, se debe considerar heparinas de bajo peso molecular o DOAC. La duración de la terapia antitrombótica estará guiada por la resolución o no del TIV en estudios de imágenes.
Figura 3: Algoritmo diagnóstico y terapéutico
(DOAC y HBPM son opciones terapéuticas si existe intolerancia a AVK)
Comentario personal:
La trombosis intraventricular es una entidad observada con elevada prevalencia en pacientes post-IAM en la era pre-ATC y pre-trombolítica, y que en la actualidad ésta ha disminuido significativamente. Se suelen observar en aquellos pacientes con IAM revascularizados de manera tardía y de gran copromiso de miocardio afectado.
Algunos puntos de discusión son, por un lado, su diagnóstico, ya que no siempre es factible su observación con ETT, es por ello que la RMC debe ser una herramienta a utilizar en aquellos casos inconclusos. Por otro lado, el tratamiento anticoagulante deben ser los AVK, que presentan evidencia más robusta, mientras que la utilización de los DOACs se han reportado en múltiples registros retrospectivos uni o multicéntricos de poca cantidad de pacientes, con resultados diversos, pero que no permiten adoptar una recomendación en su utilización sistemática. Otro tema importante en el tratamiento, es la utilización de doble o triple terapia antitrombótica, ya que la mayoría de la evidencia al respecto provienen de ensayos en pacientes con FA con IAM o sometidos a ATC; la recomendación actual es la utilización de la triple terapia el menor tiempo posible evaluando riesgo y beneficio.
Esta es una entidad clínica que posee más recomendación de expertos que evidencia de alta calidad:
-Se recomienda de rutina anticoagulación por 3 meses. ¿No deberíamos evaluar cada caso de manera individual, y así anticoagular por más o menos tiempo en función del riesgo/beneficio?
-Si la RMC es el gold standard, ¿por que no realizarlo de rutina en todos los pacientes con IAM anterior en centros con los recursos disponibles? Es probable que incremente la detección de esta entidad, e inclusive podría disminuír la tasa de eventos embólicos a largo plazo al recibir tratamiento anticoagulante.
Referencias
Massussi M., Scotti A, Lip GYH, Proietti R. Left Ventricular Thrombosis: New Perspectives on an Old Problem. Eur Heart J Cardiovasc Pharmacother. 2020 Jun 22:pvaa066. doi: http://doi.org/10.1093/ehjcvp/pvaa066
Ma S., Lu Q., Hu H., Du X. Post-infarct left ventricular thrombosis is mechanistically related to ventricular wall rupture. Medical Hypotheses 144 (2020) 109938. https://doi.org/10.1016/j.mehy.2020.109938
4 comments









































4 Comments
Gabriel parma
julio 26, 2020, 7:50 amExcelente revisión del autor de un tema muy controversia realmente y q la evidencia no acompaña, estoy de acuerdo q ante la duda la rm lo soluciona y aconsejo siempre en los isquemicos hacer realce precoz (al min) p identificarlo , y en cuanto al tto , a raíz de revisión realizada hace años y la práctica , aconsejó aco c warfarina 6 meses y re evaluar, si el trombo no está o no está móvil no protruye paro, sino sigo 6 meses y evalúo. Reitero felicitaciones al autor
REPLYGonzalo Perez@Gabriel parma
julio 26, 2020, 8:39 pmMuchas Gracias Dr. Parma por su comentario. Realmente es un tema donde no tenemos evidencia sólida que sustente el manejo. Creo que lo importante de este tema es, por un lado, que debemos anticoagular si o si a estos pacientes, y debe ser con un AVK (warfarina o acenocumarol), no indicaría DOAC. Por otro lado, el tiempo de duración, los autores recomiendan 3 meses de tratamiento y reevaluar, pero por que no menos tiempo?, si el trombo desaparece en 2 meses, no deberíamos suspender la anticoagulación? Si el trombo persiste a los 3 meses, es más sencilla la conducta, hay que continuar. Creo que 6 meses es demasiado tiempo de anticoagulación (en todos los pacientes). Saludos
REPLYEva Martinez fernandez@Gonzalo Perez
mayo 6, 2021, 1:06 pmHola
REPLYyo no soy médico .Pero he entendido perfectamente lo bien explicado aqui escrito .
Mi padre lleva 21 dias en uci .Con Infarto agudo de miocardio .Y reinfartos(2 ) .Debido al trombo y congestiòn , rotura ( jamás pense que el corazòn se pudiera romper ) …
Le operaròn a vida o muerte y le pusieron un parche cardìaco .Más tarde le hiieron una angioplastia o cateterismo ,poniendo un sten .Después antibiòticos por infecciòn .A los quince dias intentaron desentubar ( sin exito por tres veces ) .Traqueo y respirador .Bajada de golpe de frecuencia cardiaca ( 30 pulsaciones por minuto ) .Terapia con anticoagulantes y medicación para frecuencia cardiaca al alza .
Y por ùltimo ,un marcapasos .
Lo estan intentando todo .
Ahora no logran ‘que recupere ‘cociencia ‘
y mañana van ha realizarle un encefalograma y si fuese necesario un escaner …
A parte en el ventrìculo esta EL TROMBO …
Doctor que opina ?
Mil gracias .
Saludos ,Eva .
Manuel Barrera B
septiembre 16, 2021, 10:34 pmMe pareció una excelente revisión. Te felicito. En. La actualidad nosotros los manejamos con triple esquema asa, Clopidogrel, y DOAC. En trombos grandes definitivamente anticoagulacion con warfarina
REPLY