Los fármacos betabloqueantes (BB) han demostrado asociar numerosos beneficios en distintos campos de la patología cardiovascular (1)(2). En concreto, en el área de la cardiopatía isquémica, los BB han demostrado claramente su beneficio en las distintas presentaciones en la era post-reperfusión: como antianginosos en la cardiopatía isquémica crónica o reduciendo el remodelado ventricular tras un
Los fármacos betabloqueantes (BB) han demostrado asociar numerosos beneficios en distintos campos de la patología cardiovascular (1)(2). En concreto, en el área de la cardiopatía isquémica, los BB han demostrado claramente su beneficio en las distintas presentaciones en la era post-reperfusión: como antianginosos en la cardiopatía isquémica crónica o reduciendo el remodelado ventricular tras un infarto agudo que asocia disfunción ventricular izquierda(1). Sin embargo, y a colación del artículo recientemente publicado por Clemente-Moragon et al. (3), los BB, y en particular Metoprolol, en el estudio METOCARD-CNIC demostró su beneficio al administrarlo precozmente en el seno del infarto agudo de miocardio previo a la reperfusion, en términos de reducción del tamaño del infarto y mejoría de FEVI (4), y es por esto por lo que en el momento actual está indicada su administración de acuerdo con las guías de práctica clínica (5).
Así, y con el objetivo de continuar con la línea de investigación del daño por isquemia-reperfusión, el grupo liderado por el Dr. Ibáñez Cabeza demuestra que a pesar de que la reperfusión es el elemento terapeútico crucial en el tratamiento del infarto agudo, muchos pacientes quedan con un daño miocárdico importante tras la reperfusión y están en riesgo de desarrollo de insuficiencia cardiaca. Este daño ocasionado por la reperfusión se produce debido a la aparición de un edema intramiocárdico en el área reperfundida generado a expensas de la actuación de los neutrófilos(6)(7). Sin embargo, la administración precoz de metoprolol en el seno de un infarto produce un aturdimiento de los neutrófilos con la consiguiente reducción del edema tras la reperfusión y con ello disminuyendo el tamaño total del infarto (8).
De acuerdo con lo estudiado hasta este punto, metoprolol parece tener ciertas propiedades antiinflamatorias debido a su capacidad de aturdimiento sobre el neutrófilo. Con el objetivo de profundizar en el estudio de estas propiedades del metoprolol se conduce el estudio que es objeto de este comentario.
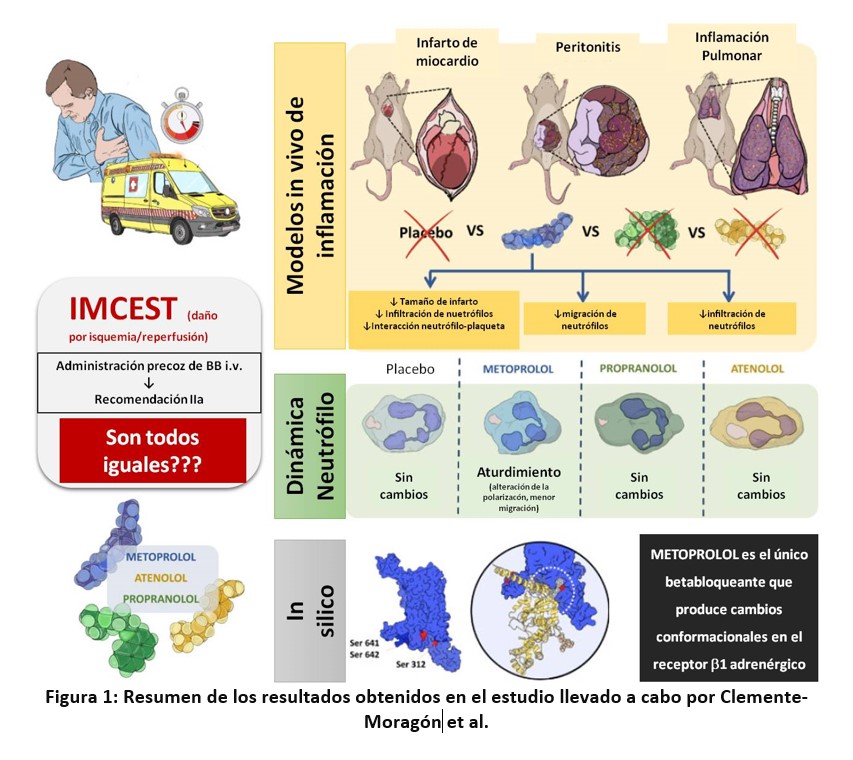
García-Clemente et al. llevan a cabo un estudio en ratones con el objeto de comparar el efecto cardioprotector de tres BB (metoprolol, atenolol y propranolol) así como de analizar el efecto que estos tres BB tienen sobre la capacidad de migración de los neutrófilos en otros modelos de inflamación en ratón como son el de peritonitis inducida por tioglicolato y el de distress respiratorio inducido por lipopolisacárido (LPS) (figura 1).
Efecto Cardioprotector de Metoprolol
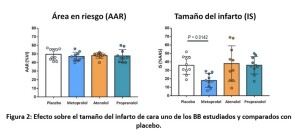
En un primer lugar para analizar el efecto cardioprotector, se utiliza un modelo de isquemia-reperfusión en el que se lleva a cabo la ligadura de la parte proximal de la arteria descendente anterior produciendo una oclusión completa de la misma durante 45 minutos para posteriormente desligar la arteria recuperando la totalidad del flujo. Previo a la reperfusión en cada uno de los grupos a comparar se administra 12,5 mg IV de metoprolol, atenolol, propranolol o placebo (suero salino). A las 24 horas de la repefusion estos animales son eutanasiados y se analiza histológicamente el área en riesgo (territorio dependiente de la irrigación por parte de la arteria descendente anterior) y el tamaño en porcentaje que representa el área necrótica con respecto al área en riesgo. Así, se observa que en los animales que recibieron placebo el área infartada representaba el 35.9% del área en riesgo, valor similar al observado en los animales que recibieron atenolol (38%) y propranolol (36%). Sin embargo el tamaño del infarto en los animales que recibieron metoprolol fue significativamente inferior con respecto a placebo (18%, p=0.0142) (figura 2). Con este hallazgo se aporta más evidencia en lo referente al efecto cardioprotector del metoprolol en el área de la isquemia-reperfusión.
Para tratar de explicar el efecto cardioprotector, se analizó en cada uno de los grupos de tratamiento la migración de neutrófilos al miocardio 24 horas tras la reperfusión mediante la determinación de la proteína Ly6G en el miocardio (biomarcador indirecto de la presencia de neutrófilos), así como la interacción neutrófilo-plaqueta, que se ha relacionado con el daño por isquemia-reperfusión, mediante la determinación en sangre periférica 24 horas post-reperfusión de células CD41-Ly6G+ (plaquetas-neutrófilos). De manera concordante solo metoprolol redujo de forma significativa la migración de neutrófilos al miocardio y la interacción plaqueta-neutrófilo post-reperfusión. Para confirmar estos datos, se decidió exponer a los neutrófilos de ratón en presencia de cada uno de los tres BB así como de placebo, a un filtro con un elemento (CXCL1) que atraía la migración del neutrófilo a través de él y contar los neutrófilos que habían migrado 90 minutos después. Se observó que con respecto a placebo solo metoprolol reducía la migración del neutrófilo a través del filtro con CXCL1 (p=0.0095).
Efecto anti-inflamatorio de metoprolol a otros niveles.
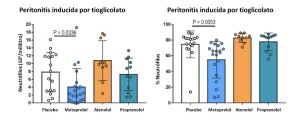
De igual manera y con las miras puestas en ver el efecto anti-inflamatorio no solo a nivel miocárdico de los BB, se analizó en un modelo en ratón de peritonitis aguda inducida por tioglicolato el número de neutrófilos que infiltraban la cavidad peritoneal en presencia de cada uno de los tres BB y de placebo, observándose que en presencia tanto de placebo como de atenolol y propranolol el número de neutrófilos que infiltraban la cavidad era claramente superior que en aquellos ratones que estaban expuestos a metoprolol (p=0,0336). Además, en este modelo de peritonitis se analizó el porcentaje de neutrófilos viables del total que había migrado a la cavidad peritoneal siendo claramente inferior en presencia de metoprolol que en presencia de placebo o de cualquiera de los otros BB (p=0.0053) (figura 3).
Figura 3: Efecto de cada uno de los BB sobre la migración de los neutrófilos en el modelo de peritonistis inducida por tioglicolato. Derecha: número total de neutrófilos en cavidad peritoneal. Izquierda: porcentaje de neutrófilos viables en cavidad peritoneal.
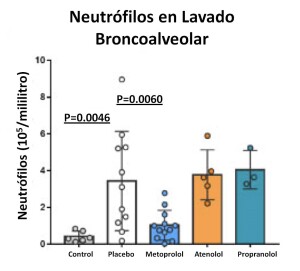
De igual manera se testeó el efecto sobre la infiltración de neutrófilos en presencia de cada uno de los tres BB y placebo en el modelo en ratón de distress respiratorio inducido por LPS. Se comprobó que en presencia de metoprolol se producía una reducción del número de neutrófilos en el lavado broncoalveolar 24 horas después de inducir el distress respiratorio con respecto a atenolol, propranolol o placebo (p=0,006)(figura 4).
Figura 4: Efecto de cada uno de los BB sobre sobre la infiltración de neutrófilos en el modelo de distress respiratorio inducido por LPS.
Así mismo, es sabido que el daño en los tejidos en el contexto de una inflamación aguda se produce por la cromatina liberada por los neutrófilos conocida como NETs (neutrophil extracelular traps). Se utilizó este modelo de distress respiratorio inducido por LPS para ver el efecto de los distintos BB sobre la formación de NETs, ya que se ha demostrado que LPS induce la formación de H3 citrulina, una proteína implicada en el desarrollo de NETs(9), y se observó que de los tres BB, solo metoprolol reduce la citrulacion de H3 y por ende la formación de NETs.
Efecto del metoprolol a nivel celular
También se analizó la velocidad de migración y la distancia recorrida por el neutrófilo en el contexto de inflamación aguda mediante la inyección de TNF-a en la capa muscular de los vasos del cremaster del ratón en presencia de placebo y de cada uno de los tres BB. Así se utilizó para ello microscopía intravital 2D observándose que sólo metoprolol reducía de forma significativa la velocidad de migración (p< 0.0001) así como la distancia recorrida por los neutrófilos (p< 0.0001).
Por último, este trabajo trata de analizar mediante estudios in silico el efecto que tienen los 3 BB a nivel de los receptores b1 adrenérgicos. Así, se demuestra que el efecto de metoprolol en la migración e infiltración de neutrófilos no sólo depende de evitar la unión de las catecolaminas al receptor b1 adrenérgico en el contexto de una inflamación aguda. Metoprolol, y no el resto de BB, produce una serie de cambios conformacionales en el receptor b1 adrenérgico: aumenta el tamaño intracelular del receptor y produce también un aumento de exposición de las serinas a la fosforilación que conlleva el aumento del reclutamiento de las b-arrestinas favoreciendo la internalización de los receptores b1 adrenérgicos y la activación de una vía de señalización que podría explicar el aturdimiento de los neutrófilos.
Sin duda se trata de un trabajo completamente novedoso en el que se demuestra que metoprolol tiene unas propiedades farmacológicas completamente distintas a otros BB y si estos resultados fueran confirmados en el terreno clínico, su uso y no el de otros BB debería de ser generalizado en el contexto de un infarto agudo previo a la reperfusión. Sin embargo, este trabajo también pone sobre la mesa que el metoprolol presenta propiedades anti-inflamatorias por el mismo mecanismo que reduce el daño por isquemia-reperfusión, es decir, mediante el aturdimiento y la consiguiente reducción en la migración e infiltración por parte de los neutrófilos de los tejidos en un proceso inflamatorio agudo. Así las cosas, este trabajo abre la puerta al estudio clínico del beneficio del uso de metorpolol en otros procesos inflamatorios como el distress respiratorio o la peritonitis.
Ver link AQUI
Referencias
1-Martinez-Milla J, Raposeiras-Roubin S, Pascual-Figal DA, Ibanez B. Role of Beta-blockers in Cardiovascular Disease in 2019. Rev Esp Cardiol (Engl Ed). 2019 Oct;72(10):844–52.
2-Ibáñez B, Raposeiras-Roubin S, García-Ruiz JM. The Swing of β-Blockers. J Am Coll Cardiol. 2017 Jun 6;69(22):2721–4.
3-Clemente-Moragón A, Gómez M, Villena-Gutiérrez R, Lalama D V, García-Prieto J, Martínez F, et al. Metoprolol exerts a non-class effect against ischaemia–reperfusion injury by abrogating exacerbated inflammation. Eur Heart J [Internet]. 2020 Oct 7; Available from: https://doi.org/10.1093/eurheartj/ehaa733
4-Ibanez B, Macaya C, Sanchez-Brunete V, Pizarro G, Fernandez-Friera L, Mateos A, et al. Effect of early metoprolol on infarct size in ST-segment-elevation myocardial infarction patients undergoing primary percutaneous coronary intervention: the Effect of Metoprolol in Cardioprotection During an Acute Myocardial Infarction (METOCARD-CNIC) tri. Circulation. 2013 Oct;128(14):1495–503.
5-Ibanez B, James S, Agewall S, Antunes MJ, Bucciarelli-Ducci C, Bueno H, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevationThe Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society. Eur Heart J. 2018;39(2):119–77.
6-Fernandez-Jimenez R, Sanchez-Gonzalez J, Aguero J, Garcia-Prieto J, Lopez-Martin GJ, Garcia-Ruiz JM, et al. Myocardial edema after ischemia/reperfusion is not stable and follows a bimodal pattern: imaging and histological tissue characterization. J Am Coll Cardiol. 2015 Feb;65(4):315–23.
7-Fernandez-Jimenez R, Garcia-Prieto J, Sanchez-Gonzalez J, Aguero J, Lopez-Martin GJ, Galan-Arriola C, et al. Pathophysiology Underlying the Bimodal Edema Phenomenon After Myocardial Ischemia/Reperfusion. J Am Coll Cardiol. 2015 Aug;66(7):816–28.
8-García-Prieto J, Villena-Gutiérrez R, Gómez M, Bernardo E, Pun-García A, García-Lunar I, et al. Neutrophil stunning by metoprolol reduces infarct size. Nat Commun. 2017;8:14780.
9-Liu S, Su X, Pan P, Zhang L, Hu Y, Tan H, et al. Neutrophil extracellular traps are indirectly triggered by lipopolysaccharide and contribute to acute lung injury. Sci Rep [Internet]. 2016;6(1):37252. Available from: https://doi.org/10.1038/srep37252









































Deje un comentario
Registrese para comentar. Sus e-mail no será publicados