La Asociación de Insuficiencia Cardíaca de la Sociedad Europea de Cardiología propone, en este documento, identificar nueve fenotipos de necesidades individuales de titulación ascendente en pacientes con insuficiencia cardíaca y fracción de eyección reducida. El tratamiento de pacientes con insuficiencia cardíaca (IC) y fracción de eyección reducida (IC- FER) está muy bien respaldado por grandes
La Asociación de Insuficiencia Cardíaca de la Sociedad Europea de Cardiología propone, en este documento, identificar nueve fenotipos de necesidades individuales de titulación ascendente en pacientes con insuficiencia cardíaca y fracción de eyección reducida.
El tratamiento de pacientes con insuficiencia cardíaca (IC) y fracción de eyección reducida (IC- FER) está muy bien respaldado por grandes ensayos clínicos aleatorizados (ECA) que sustentan las recomendaciones de las guías de manejo. (1-3) A pesar de la evidencia, la implementación de las recomendaciones es deficiente. Una porción importante de los pacientes no reciben el tratamiento farmacológico completo o a las dosis adecuadas, que han demostrado tener un impacto en la morbimortalidad. Y este incumplimiento de las recomendaciones de la terapia médica dirigida por las guías (TMDG) por parte de los médicos, se ha asociado con mayor mortalidad. (4)
Históricamente, el tratamiento de pacientes con IC-FER incluyó inhibidores de la enzima convertidora de angiotensina (IECA) o bloqueadores del receptor de angiotensina (BRA), betabloqueantes (BB), antagonistas de los receptores de mineralocorticoides (ARM), digoxina, diuréticos y dispositivos. Durante la última década se ha demostrado un impacto positivo en la mortalidad y/o la morbilidad con la incorporación de ivabradina, sacubitrilo/valsartán, inhibidores del cotransportador-2 de sodio y glucosa (iSGLT2), carboximaltosa férrica, vericiguat y omecamtiv mecarbil.
Este concepto de terapia múltiple ha generado que expertos y sociedades científicas de diferentes latitudes hayan propuesto, en los meses recientes, diferentes esquemas de inicio y progresión en la titulación de los fármacos. Como ya se ha propuesto en este espacio, el inicio del tratamiento de la IC no debe ser visto como una aporía (sin salida) sino como un dilema, donde existen distintos caminos a seguir, vertical u horizontal, combinado o secuencial. (5) Con esta premisa, deberíamos priorizar una terapia combinada, pero personalizada al fenotipo clínico del paciente.
El más reciente de estos documentos es un Consenso de la Asociación de Insuficiencia Cardíaca de la Sociedad Europea de Cardiología (HFA-ESC) que analiza los perfiles de pacientes de IC-FER para adaptar la terapia médica, reconociendo las causas del subtratamiento. (1) Además de «factores no médicos» como el bajo nivel socioeconómico, la falta de apoyo social y la mala adherencia, se identificaron factores médicos, biológicos, como son la presión arterial (PA) baja, la frecuencia cardíaca (FC), la fibrilación auricular (FA), la disfunción renal, los niveles de potasio y grado de congestión. Estos factores limitan, muchas veces, la implementación y el ajuste ascendente de la TMDG en la IC-FER.
La estratificación de los pacientes con IC es un permanente desafío, ya que existe una superposición de fenotipos clínicos en todo el espectro de la enfermedad. Con el surgimiento de nuevos fármacos eficaces, la demanda de fenotipado se ha vuelto cada vez más importante debido en parte a que algunos pacientes no tolerarán todos los medicamentos.
Los beneficios demostrados por los ECA en los tratamientos de la IC-FER involucran a una población seleccionada que no incluyen mayoritariamente a pacientes mayores, frágiles y multimórbidos como los que atendemos en el mundo real. Además, los ECA han excluido a los pacientes con PA, FC y tasa de filtrado glomerular (TFGe) bajas, y han abordado la titulación de la medicación de forma estandarizada. Por esa razón, hoy resulta importante para llenar este vacío en la evidencia, analizar los resultados de los registros, que sugieren beneficios de la TMDG en una población más amplia. (6, 7) Los pacientes con IC tienen muchas presentaciones diferentes en cuanto a congestión, estado hemodinámico y función renal. Por lo tanto, ajustar o priorizar los medicamentos de acuerdo con el perfil de los pacientes parece una forma razonable de brindar a cada paciente individual el beneficio de la TMDG.
Por otra parte, los pacientes con IC rara vez son naïve con respecto a las terapias farmacológicas y ya suelen recibir IECA, BB o diuréticos debido a hipertensión, cardiopatía isquémica, FA u otras afecciones. Otro escenario clínico frecuente es el del paciente hospitalizado por IC en los que se redujo o suspendió la TMDG. Las barreras para la implementación de la terapia, se manifiestan especialmente en la “fase vulnerable” posterior al alta hospitalaria por un episodio de descompensación de la IC. (8)
El desafío es priorizar adecuadamente o elegir la titulación ascendente de medicamentos más adecuada de acuerdo con el perfil de los pacientes. Sin lugar a dudas, todos los pacientes deberían recibir el tratamiento básico para la IC que ha demostrado reducir las hospitalizaciones y la mortalidad. El núcleo de la TMDG de la IC-FER incluye 4 grupos de fármacos: BB, IECA/BRA/ARNI, ARM e iSGLT2.
Estos fármacos mejoran claramente el pronóstico, pero afectan, en forma variable, la PA, la FC, la función renal y los niveles de potasio. La congestión puede afectar negativamente la titulación adecuada de la TMDG, por lo que en primer lugar se deben dosificar los diuréticos en el régimen correcto para lograr un estado euvolémico. Ante esta situación compleja, la identificación de los fenotipos del paciente ayuda a identificar estrategias terapéuticas personalizadas.
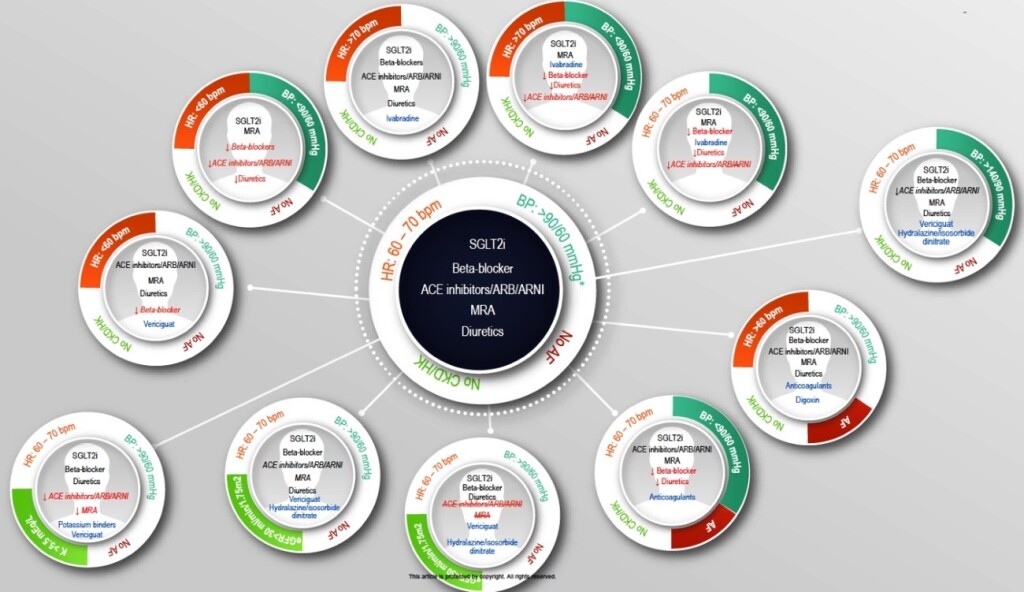
La HFA-ESC propone, en este documento, identificar nueve fenotipos de pacientes con necesidades individuales de titulación ascendente. (1) (Figura).
Figura – Adaptación de la terapia médica según perfiles clínicos. (1)
Según las características de algunos pacientes (BP: presión arterial; HR: frecuencia cardíaca; AF: presencia de fibrilación auricular; CKD: enfermedad renal crónica; HK: hiperkalemia), es posible que haya que reducir, suspender o añadir algunos fármacos.
En negro: medicamentos que deben administrarse.
En rojo: medicamentos que deben reducirse o suspenderse.
En azul: medicamentos que deben agregarse.
1)Pacientes con PA baja y FC alta.
-No existe una definición clara de PA baja en la IC, pero en general se acepta una presión arterial sistólica (PAS) <90 mmHg. Sin embargo, en pacientes con enfermedad coronaria se recomienda una PAS >120 mmHg. (9)
-Evaluar y corregir causas de hipotensión arterial: hipovolemia, sangrado, infección.
-Considerar suspender otros medicamentos hipotensores no imprescindibles (nitratos, bloqueantes cálcicos, otros vasodilatadores).
-Diuréticos: si el paciente se encuentra euvolémico, se puede intentar la reducción o suspensión con vigilancia cuidadosa en los días siguientes para evitar la retención de líquidos.
-La modificación de la medicación TMDG o sus dosis debe abordarse sólo si el paciente tiene hipotensión sintomática.
-Sacubitrilo/valsartán: no se recomienda en pacientes con presión arterial sistólica <100 mmHg.
-ARM e iSGLT2: tienen un impacto muy modesto en la presión arterial, por lo que su suspensión no es necesaria.
-Lograr una FC más baja se asocia con una mejor supervivencia en IC-FER y ritmo sinusal. El resultado más favorable se observa con una FC de alrededor de 60 lpm. (10)
-BB: deben ajustarse a la dosis máxima tolerada.
-Ivabradina: si hay hipotensión sintomática, puede ser necesaria la reducción o suspensión de BB. En esta situación, la ivabradina en combinación de un BB permite alcanzar dosis más altas de ambos fármacos que la titulación aislada. (11)
-Omecamtiv mecarbil: parece una opción terapéutica interesante en los pacientes más gravemente afectados dentro de este fenotipo.
2-Pacientes con PA baja y FC baja
-Considerar otras causas de hipotensión y medicamentos hipotensores.
-La modificación de la medicación TMDG o sus dosis debe abordarse sólo si el paciente tiene hipotensión sintomática.
-ARM e iSGLT2: tienen un impacto muy modesto sobre la PA, por lo que su suspensión es innecesaria.
-BB: puede ser necesaria reducir la dosis si el paciente tiene una FC <50 lpm o bradicardia sintomática.
-Omecamtiv mecarbil: es una opción terapéutica viable en estos pacientes cuando la TMDG se encuentra limitada.
3-Pacientes con PA normal y FC baja
-Considerar suspender otros medicamentos con un efecto cronotrópico negativo (bloqueantes cálcicos no dihidropiridínicos, digoxina, antiarrítmicos).
-Ivabradina: reducir su dosis o suspender si la FC permanece <50 lpm o el paciente tiene bradicardia sintomática.
-BB: pacientes con FC <50 lpm o bradicardia sintomática también requerirán una reducción de la dosis.
-Pacientes con PA normal y FC alta
-BB: deben ser titulados en alta a la dosis objetivo.
-Ivabradina: debe adicionarse si persista FC alta en ritmo sinusal (FC >70 lpm) lo que conduce a un mejor control de la FC y una mejor titulación de BB con una menor incidencia de efectos secundarios. (11)
-IECA/BRA/ARNI: deben ajustarse hacia arriba a la dosis objetivo.
-Vericiguat: en pacientes hospitalizados considerarlo antes del alta.
-Pacientes con FA y PA normal
-No se ha determinado cuál es la frecuencia ventricular óptima de reposo en pacientes con FA e IC, pero puede estar entre 70 y 80 lpm. (12) Las FC <70 lpm se asociaron con un peor resultado en pacientes con FA.
-A diferencia de los pacientes en ritmo sinusal, la FC no es un predictor de mortalidad en pacientes con IC-FEr y FA.
-BB: no hay evidencia clara de un beneficio pronóstico de los BB en pacientes con IC y FA. (12, 13)
-Anticoagulación (preferiblemente con NOAC): siempre está indicada en pacientes con FA a menos que los riesgos superen los beneficios potenciales o estos fármacos tengan una contraindicación específica.
-Pacientes con FA y PA baja
-Debe mantenerse una FC >70 lpm. (12)
-BB: como la evidencia del beneficio sobre la mortalidad y la morbilidad es menos fuerte, pueden reducirse o suspenderse si es necesario. (12, 13)
-Digoxina: puede utilizarse para el control de la FC, como una alternativa al BB, ya que no tiene efectos sobre la PA. Esta estrategia puede permitir la introducción o revalorización de fármacos con impacto en la mortalidad y morbilidad, como IECA o ARNI.
-ARM e iSGLT2: tienen un impacto muy modesto en la PA, por lo que su suspensión no es obligatoria ni necesaria.
-Anticoagulación (preferiblemente con NOAC): siempre está indicada en pacientes con FA a menos que estén contraindicados.
-Pacientes con enfermedad renal crónica
-La mayoría de los ECA excluyen a los pacientes con enfermedad renal crónica (ERC) grave, lo que limita la evidencia disponible sobre el beneficio y la seguridad de los fármacos. Sin embargo, datos derivados de registros muestran que estos pacientes podrían beneficiarse potencialmente de la TMDG.
-Suspender otros fármacos que pueden empeorar la función renal (AINEs).
-BB: pueden administrarse de forma segura a pacientes con una TFGe <30 ml/min/1,73 m2, con un claro beneficio en la mortalidad.
-IECA/ARB/ARNI: sólo deben interrumpirse cuando la creatinina aumenta >100% o >3,5 mg/dL o TFGe <20 ml/min/1,73 m2.
-Sacubitrilo/valsartán: puede usarse hasta una TFGe <30 ml/min/1,73 m2.
-ARM: se pueden administrar hasta una TFGe de 30 ml/min/1,73 m2, siempre que el potasio sea ≤ 5,0 mEq/L.
-Realizar análisis de niveles de potasio 1 y 4 semanas después de comenzar o aumentar la dosis de ARM y periódicamente a partir de entonces.
-iSGLT2: Existe evidencia de beneficio y seguridad y mejoría de los puntos finales cardiovasculares y renales en pacientes con una TFGe >20-25 ml/min/1,73 m2.
-La pequeña caída de la TFGe en los primeros días después del inicio de un iSGLT2 no debe provocar el cese de esta terapia, ya que esta reducción es reversible y se asocia con beneficio a largo plazo de la función renal. (14)
-Vericiguat: se pueden administrar a pacientes con TFGe >15 ml/min/1,73 m2.
-Omecamtiv mecarbil: se pueden administrar a pacientes con TFGe >20 ml/min/1,73 m2.
-Quelantes de potasio (patirómero y ciclosilicato de sodio y circonio): han demostrado eficacia reduciendo el potasio sérico en pacientes con IC y ERC tratados con iSRAA (15). Sin embargo, todavía no hay evidencia de su impacto positivo en el pronóstico.
-Paciente previo al alta
-Aproximadamente un tercio de los pacientes son dados de alta de una hospitalización por IC con signos clínicos de congestión residual.
-BB: el inicio en un paciente congestivo que no los recibía previamente puede conducir a un deterioro clínico por lo que, en estos casos, los BB no deben ser la primera línea de tratamiento.
-ARNI: en pacientes que ya habían recibido un IECA deben iniciarse primero, siempre que el paciente tenga una PAS >100 mmHg. (16, 17)
-ARM e iSGLT2: pueden introducirse de forma segura, incluso en pacientes congestivos y con PA baja. La empagliflozina fue bien tolerada en estos pacientes y redujo el criterio de valoración combinado de empeoramiento de la IC, rehospitalización por IC o muerte a los 60 días. (18). En pacientes diabéticos hospitalizados por IC, la sotagliflozina redujo el criterio de valoración combinado de mortalidad cardiovascular y hospitalizaciones y visitas urgentes por IC, cuando se inició antes o justo después del alta. (19)
-Omecamtiv mecarbil y vericiguat: se pueden utilizar en pacientes seleccionados antes del alta, ya que han demostrado reducir los eventos. Pueden contribuir a la descongestión, permitiendo eventualmente un inicio más seguro de BB.
-Paciente con hipertensión a pesar de GDMT
-Evaluar otros fármacos que pueda aumentar la presión arterial (AINEs, corticoides, broncodilatadores).
-Asegurar la adherencia de los pacientes a la medicación y el uso de las dosis más altas recomendadas de la TMDG.
-Dinitrato de isosorbide e hidralazina: se debe utilizar esta combinación si, a pesar de TMDG en dosis óptimas, el paciente persiste hipertenso.
Conclusión
Se deben hacer todos los esfuerzos posibles para iniciar y aumentar la terapia básica que tiene impacto importante y concluyente en la mortalidad y morbilidad de los pacientes con IC-FER. Un enfoque personalizado del paciente, ajustando la TMDG al perfil hemodinámico del paciente (PA, FC, congestión) y la función renal, puede permitir lograr un mejor y más completo tratamiento para cada paciente individual. Seguramente será mejor que el sistema secuencial tradicional de titulación forzada estandarizada o de un enfoque rígido de “talla única”.
Existe una necesidad insatisfecha de ECA que incluyan más pacientes de la vida real y prueben diferentes estrategias para lograr un tratamiento integral. La investigación actual debería dirigirse hacia estos fenotipos no explorados suficientemente.
Ver link AQUI
Bibliografía:
1.Rosano G, Moura B, Metra M, Bauersachs J, Ben Gal T, Adamopoulos S, et al. Patients profiling in Heart Failure for tailoring medical therapy. A consensus document of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2021 May 1.doi:10.1002/ejhf.2206.
2.Ponikowski P, Voors A, Anker S, Bueno H, Cleland J, Coats A, et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur J Heart Fail 2016; 18:891-975. doi:10.1002/ejhf.592.
3.Seferovic P, Ponikowski P, Anker S, Bauersachs J, Chioncel O, Cleland J, et al. Clinical practice update on heart failure 2019: pharmacotherapy, procedures, devices and patient management. An expert consensus meeting report of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2019; 21:1169-1186. doi:10.1002/ejhf.1531.
4.Komajda M, Schöpe J, Wagenpfeil S, Tavazzi L, Böhm M, Ponikowski P, et al. Physicians’ guideline adherence is associated with long-term heart failure mortality in outpatients with heart failure with reduced ejection fraction: the QUALIFY international registry. Eur J Heart Fail 2019; 21:921-929. doi:10.1002/ejhf.1459.
5.Perna ER, Jerez Castro AM, Coronel ML. Aporía o dilema: Cómo iniciar el tratamiento de la insuficiencia cardíaca con fracción de eyección reducida. SIAC May-2021. https://www.siacardio.com/consejos/falla-cardiaca/aporia-o-dilema-como-iniciar-el-tratamiento-de-la-insuficiencia-cardiaca-con-fraccion-de-eyeccion-reducida/
6.Stolfo D, Uijl A, Benson L, Schrage B, Fudim M, Asselbergs F, et al. Association between beta-blocker use and mortality/morbidity in older patients with heart failure with reduced ejection fraction. A propensity score-matched analysis from the Swedish Heart Failure Registry. Eur J Heart Fail 2020; 22:103-112. doi:10.1002/ejhf.1615.
7.Savarese G, Dahlström U, Vasko P, Pitt B, Lund L. Association between renin-angiotensin system inhibitor use and mortality/morbidity in elderly patients with heart failure with reduced ejection fraction: a prospective propensity score-matched cohort study. Eur Heart J 2018; 39:4257-4265. doi:10.1093/eurheartj/ehy621.
8.Calvin J, Shanbhag S, Avery E, Kane J, Richardson D, Powell L. Adherence to evidence-based guidelines for heart failure in physicians and their patients: lessons from the Heart Failure Adherence Retention Trial (HART). Congest Heart Fail 2012; 8:73-8. doi:10.1111/j.1751-7133.2011.00263.x.
9.Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J 2018; 39:3021–3104. org/10.1093/eurheartj/ehy339.
10.Swedberg K, Komajda M, Böhm M, Borer J, Ford I, Dubost-Brama A, et al. SHIFT Investigators. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet 2010; 376:875-85. doi:10.1016/S0140-6736(10)61198-1.
11.Volterrani M, Cice G, Caminiti G, Vitale C, D’Isa S, Perrone Filardi P, et al. Effect of Carvedilol, Ivabradine or their combination on exercise capacity in patients with Heart Failure (the CARVIVA HF trial). Int J Cardiol 2011; 151:218-24. doi:10.1016/j.ijcard.2011.06.098.
12.Bauersachs J, Veltmann C. Heart rate control in heart failure with reduced ejection fraction: the bright and the dark side of the moon. Eur J Heart Fail 2020; 22:539-542. doi:10.1002/ejhf.1733.
13.Kotecha D, Holmes J, Krum H, Altman DG, Manzano L, Cleland J, et al. Beta-Blockers in Heart Failure Collaborative Group. Efficacy of β blockers in patients with heart failure plus atrial fibrillation: an individual-patient data meta-analysis. Lancet 2014; 384:2235-43. doi:10.1016/S0140-6736(14)61373-8.
14.Heerspink H, Stefánsson B, Correa-Rotter R, Chertow G, Greene T, Hou F, et al. DAPA-CKD Trial. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med 2020; 383:1436-1446. doi:10.1056/NEJMoa2024816.
15.Rosano G, Tamargo J, Kjeldsen K, Lainscak M, Agewall S, Anker S, et al. Expert consensus document on the management of hyperkalaemia in patients with cardiovascular disease treated with renin angiotensin aldosterone system inhibitors: coordinated by the Working Group on Cardiovascular Pharmacotherapy of the ESC. Eur Heart J Cardiovasc Pharmacother 2018; 4:180-188. doi:10.1093/ehjcvp/pvy015.
16.Velazquez E, Morrow D, DeVore A, Duffy C, Ambrosy A, McCague K, et al. PIONEER-HF Investigators. Angiotensin-Neprilysin Inhibition in Acute Decompensated Heart Failure. N Engl J Med 2019; 380:539-548. doi:10.1056/NEJMoa1812851.
17.Wachter R, Senni M, Belohlavek J, Straburzynska-Migaj E, Witte K, Kobalava Z, et al. Initiation of sacubitril/valsartan in haemodynamically stabilised heart failure patients in hospital or early after discharge: primary results of the randomised TRANSITION study. Eur J Heart Fail 2019; 21:998-1007. doi:10.1002/ejhf.1498.
18.Damman K, Beusekamp J, Boorsma E, Swart H, Smilde T, Elvan A, et al. Randomized, double-blind, placebo-controlled, multicentre pilot study on the effects of empagliflozin on clinical outcomes in patients with acute decompensated heart failure (EMPA-RESPONSE-AHF). Eur J Heart Fail 2020; 22:713-722. doi:10.1002/ejhf.1713.
19.Bhatt D, Szarek M, Steg P, Cannon C, Leiter L, McGuire D, et al. SOLOIST-WHF Trial Investigators. Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure. N Engl J Med 2020 Nov 16. doi:10.1056/NEJMoa2030183.








































Deje un comentario
Registrese para comentar. Sus e-mail no será publicados