Una reciente publicación de la revista europea de cardiología en la sección ¨Clinical Review¨ por Halliday et al. (1) realiza un análisis de mucho interés con respecto de la valoración de la función sistólica ventricular izquierda desde la imagen cardiaca. Esta, tradicionalmente ha sido evaluada mediante el cálculo de la fracción de eyección del ventrículo
Una reciente publicación de la revista europea de cardiología en la sección ¨Clinical Review¨ por Halliday et al. (1) realiza un análisis de mucho interés con respecto de la valoración de la función sistólica ventricular izquierda desde la imagen cardiaca. Esta, tradicionalmente ha sido evaluada mediante el cálculo de la fracción de eyección del ventrículo izquierdo (FEVI). Dicho parámetro es el mayormente utilizado en la práctica rutinaria en distintos escenarios clínicos para la toma de conductas; sin embargo, ha demostrado ser un pobre predictor pronóstico en otros campos, como la insuficiencia cardiaca (IC) con FEVI preservada, así como enfermedades infiltrativas como la amiloidosis cardiaca o pacientes con patología valvular, en donde puede existir disfunción de la fibra miocárdica a pesar de una FEVI estimada como normal. La valoración del strain miocardico es una técnica prometedora que permite el estudio de la deformación de la fibra miocárdica como un estimador de disfunción sistólica subclínica que intenta mejorar las limitaciones antes mencionadas. La medición del strain miocárdico, especialmente el strain longitudinal global (SLG) ha demostrado consistentemente que puede mejorar la estratificación del riesgo de los pacientes con insuficiencia cardíaca e identifica individuos con escenarios clínicos diversos que tienen descompensación miocárdica a pesar de tener una FEVI conservada y por ende, un mayor riesgo de eventos adversos.
Precisión en la estimación de los volúmenes y la FEVI
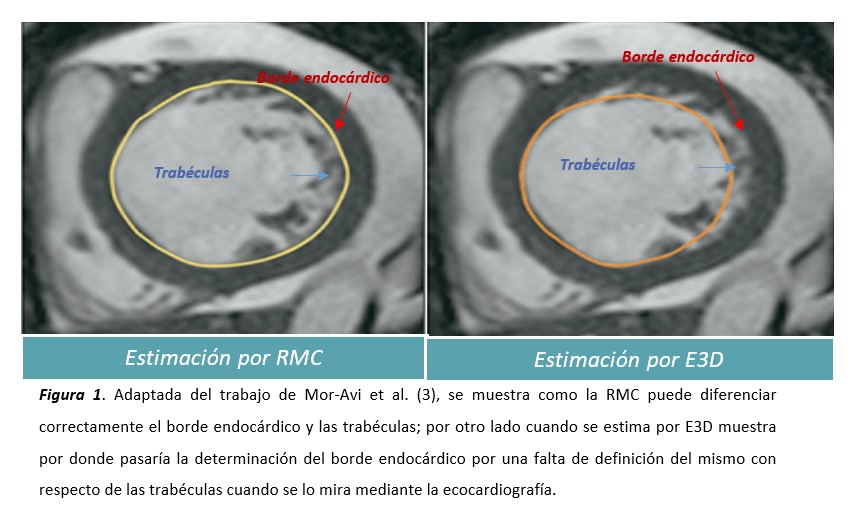
La era moderna de la imagen cardiovascular multimodal, nos ha permitido determinar la precisión de los distintos métodos disponibles para la cuantificación de volúmenes del VI y la FEVI. Aunque disponemos de varios métodos de imagen, la resonancia magnética cardíaca (RMC) se considera la modalidad más precisa para tal fin y se reconoce como el estándar de oro. Su principal fortaleza radica en la correcta visualización y determinación del borde endocárdico que permite un cálculo más preciso y con menor variabilidad de su estimación entre operadores (2). Sin embargo, la ecocardiografía es actualmente el método generalmente utilizado en la práctica clínica, principalmente debido a la amplia disponibilidad, distribución y rápida adquisición. Sin embargo, tiene varias debilidades intrínsecas: es dependiente del operador, la variabilidad para su estimación intra y entre observadores ha demostrado estar cercana a los 10 puntos porcentuales, realiza asunciones geométricas y está supeditada a una correcta visualización y determinación del borde endocárdico que no siempre es factible. Cuando la ventana ultrasónica es adecuada, la ecocardiografía tridimensional (E3D) es una modalidad más reproducible y precisa para la evaluación de los volúmenes y FEVI. Se ha demostrado que cuando se compara la precisión de la E3D contra la RMC; la E3D subestima los volúmenes, toda vez que no puede visualizar en forma precisa el borde endocárdico ventricular, esto trae consigo un error sistemático en la estimación de estos parámetros (3) (figura 1)
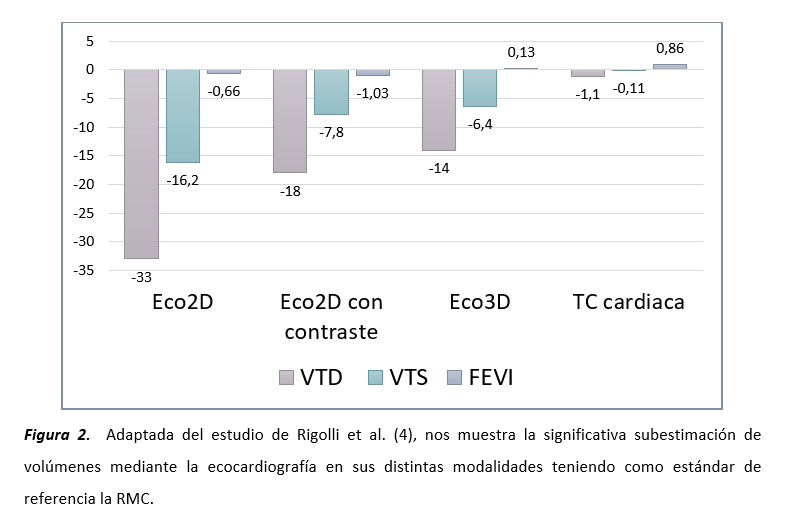
A pesar de esto, la E3D ha demostrado en un meta-análisis de 65 estudios de 2888 pacientes, ser la técnica de la ecocardiografía con menor tasa de subestimación de los volúmenes comparada contra la Eco2D y la Eco2D con contraste (4). Por otro lado, la tomografia computada cardiaca ofrece la mejor precisión para el cálculo de los volúmenes comparado contra otras técnicas, teniendo como el estandar de referencia la RMC (Figura 2). Independiente del método utlizado, es importante tener en cuenta que falta estandarización de la medición de la FEVI en muchos ensayos clínicos y la variación en precisión y exactitud entre los métodos utilizados al seleccionar pacientes para tratamientos basados en valores de técnicas contemporáneas como el E3D, la RMC y la tomografía computada cardiaca.
La función sistólica más allá de la fraccion de eyección: La incorporación del strain miocárdico al estudio de la función ventricular
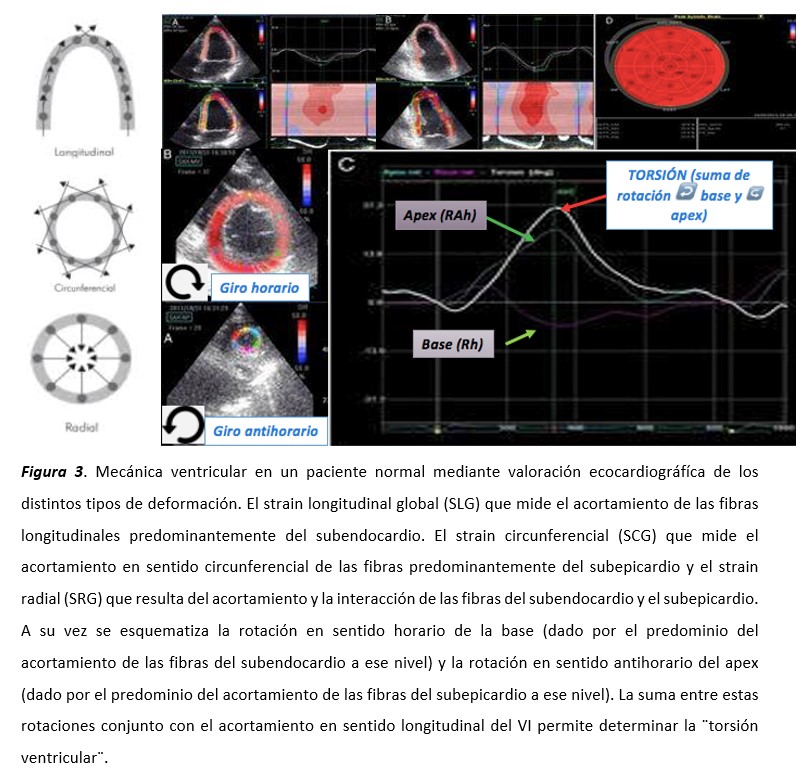
Como ya se mencionó, en determinados escenarios la FEVI no es capaz de expresar la disfunción sistólica ventricular miocárdica más allá de la precisión que podamos tener para su estimación con distintas técnicas de la imagen cardiaca. La FEVI en realidad, responde a una compleja interacción de varios tipos de fibras miocardicas con distinta disposición y orientación dentro del corazón, que ha sido demostrado mediante estudios de disección miocárdica, anatomía patológica y más recientemente con técnicas avanzadas de experimentación de la RMC con tensor de difusión (5,6). Podemos intentar resumir diciendo que el VI está dispuesto de dos tipos de fibras con distinta disposición y orientación; las fibras descendentes que predominan en el subendocardio encargadas del acortamiento en sentido longitudinal y las fibras ascendentes del subepicardio encargadas del acortamiento en sentido circunferencial. El agonismo-antagonismo, es decir, la interacción de estas fibras durante el ciclo cardiaco son determinantes de la FEVI. Si contamos por separado el grado de acortamiento de estas fibras están en el orden del 15-20% como máximo. Si la eyección fuera simplemente el resultado de la contracción independiente de cada tipo de fibra, la fracción de eyección sería cercana al 15-20%, cuando sabemos que la FEVI real es cercana al 60-70%. Esto se puede explicar debido a la interacción de ambas tipos de fibras miocárdicas. El acortamiento simultáneo permite además, que los segmentos más basales del VI giren con rotación horaria (por un predominio del acortamiento de las fibras del subendocardio en esa región) y que el apex lo haga con rotación antihoraria (por un predominio del acortamiento de las fibras del subepicardio en esa región), este fenómeno se conoce como ¨torsión ventricular¨: contracción y acortamiento de las fibras a la vez de una acción de retorcimiento simultáneo que permite explicar una FEVI del 60-70% (7) (figura 3).
La mayoría de las fibras orientadas longitudinalmente, se encuentran en el subendocardio y son más susceptibles a la enfermedad miocárdica, incluida la isquemia. Muchos estudios han demostrado que el SLG detecta anormalidades del acortamiento longitudinal que no afectan la FEVI en forma global. Probables efectos compensatorios han demostrado ser los responsables en este escenario de mantener una FEVI preservada. Stokke et al. (8) demostró que las fibras circunferenciales en la pared media, pueden compensar la pérdida de la mecánica longitudinal para preservar la función de la bomba del VI. El aumento del grosor de la pared y/o la reducción del volumen de diástole podrían explicar una FEVI normal a pesar de la reducción del acortamiento. Por lo cual, se describe que la FEVI es menos sensible a la pérdida en el acortamiento longitudinal, es decir a la disminución del SLG. Un escenario clínico representativo de este comportamiento es la amiloidosis cardiaca, en donde la FEVI es normal y existe disminución del SLG del VI (figura 4).
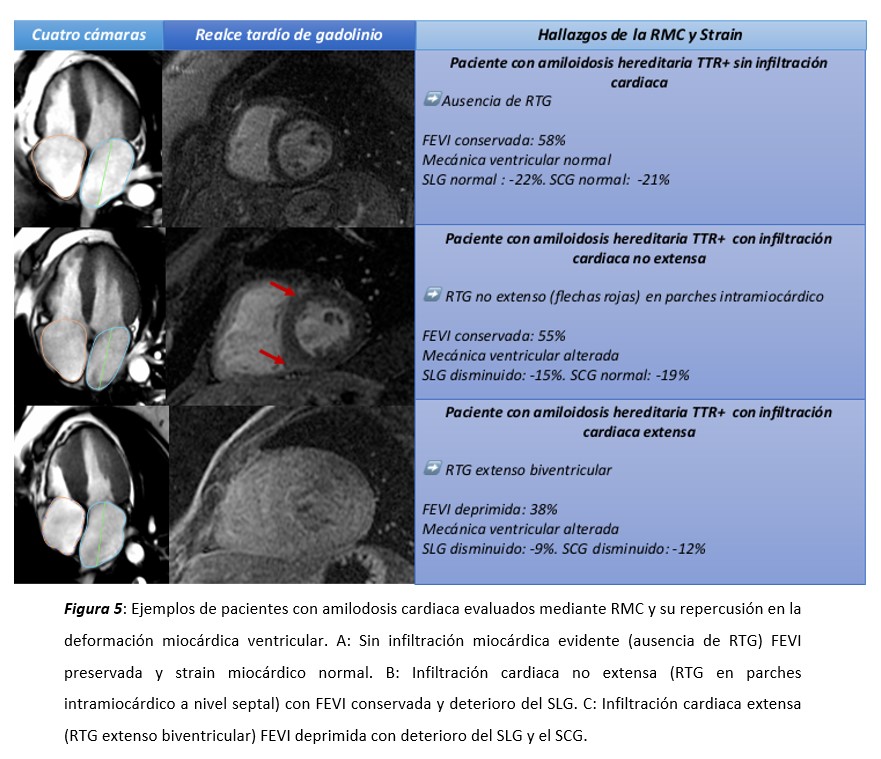
Esto puede ser explicado por los mecanismos de adaptación de las fibras miocárdicas antes mencionado, en donde los fenómenos de acortamiento circunferencial y el twist apical que puede estar normal o incrementado, permite mantener la FEVI dentro de valores normales. A medida que avanza la enfermedad y la infiltración aumenta, dichos mecanismos compensatorios se acaban y en el estadio avanzado de la enfermedad se pondrá en evidencia el deterioro de la FEVI y la caída de todos los tipos de strain y la torsión. Por otro lado, la imagen por RMC nos permitirá el estudio del grado de infiltración miocárdica mediante la determinación de la distribución del realce tardío de gadolinio en estos pacientes. A medida que aumenta el grado de infiltración, será mayormente probable el deterioro de la FEVI (figura 5).
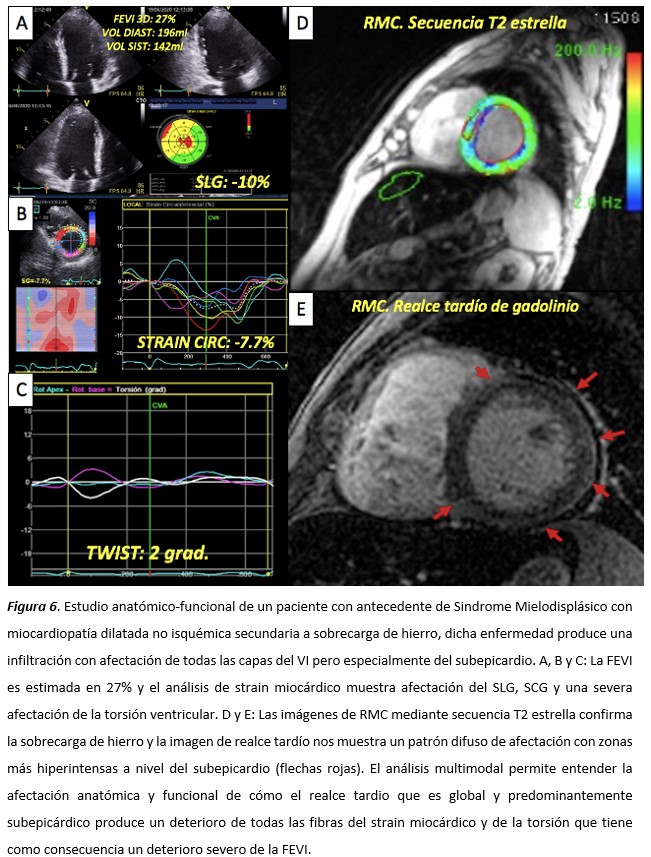
El realce tardío con gadolinio de la RMC es una técnica robusta que nos permite el estudio y la discriminación etiológica de las miocardiopatías, siendo la expresión de la fibrosis focal instaurada en el miocardio ventricular. La relación entre los hallazgos de la distribución del realce tardío desde la RMC en patrones como del subendocardio o subepicardio y sus implicancias con respecto del strain miocárdico no está del todo establecida. Creemos que la integración de ambas imágenes permitirá entender los hallazgos anatómicos y funcionales de la afectación ventricular mediante la valoración de la fibrosis de la RMC con respecto del compromiso de las distintas fibras del strain miocárdico (figura 6).
Limitaciones y utilidades clínicas
El uso del strain circunferencial y radial tiene limitada data de validación y variabilidad entre distintos proveedores en múltiples escenarios clínicos. El SLG ha sido la técnica con mayor validación in vivo e in vitro por microsonometría y en la práctica clínica. Sin embargo, es importante mencionar que a pesar de que el SLG es un método que ha mostrado una menor variabilidad intraobservador en su estimación, existe a la fecha una falta de estandarización de valores normales y patológicos entre distintas marcas y modelos de equipos, por lo cual se requieren más estudios que permitan su generalización para su uso en la práctica clínica habitual. Por otro lado, la evaluación de la deformación en forma regional y no global ha sido más dificil de reproducir en forma consistente (1).
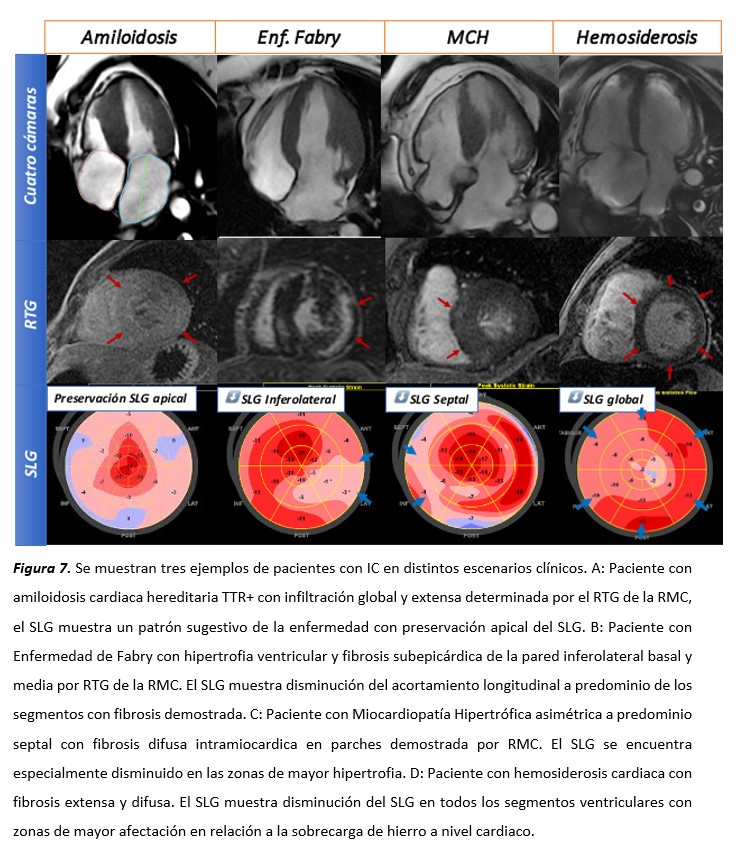
Una de las utilidades del SLG en pacientes que se presentan con insufiencia cardiaca es la aproximación etiológica de la entidad subyacente tanto en IC con FEVI preservada como con FEVI reducida (Figura 7). Distintos patrones se pueden correlacionar con los hallazgos de la fibrosis observada mediante el realce tardío de gadolinio de la RMC. Dicha aproximación mediante el SLG es importante a fin de determinar pacientes que recibirán tratamientos específicos en escenarios como la Amiloidosis cardiaca o enfermedades de depósito como la enfermedad de Fabry o la sobrecarga de hierro cardiaco, entre otras.
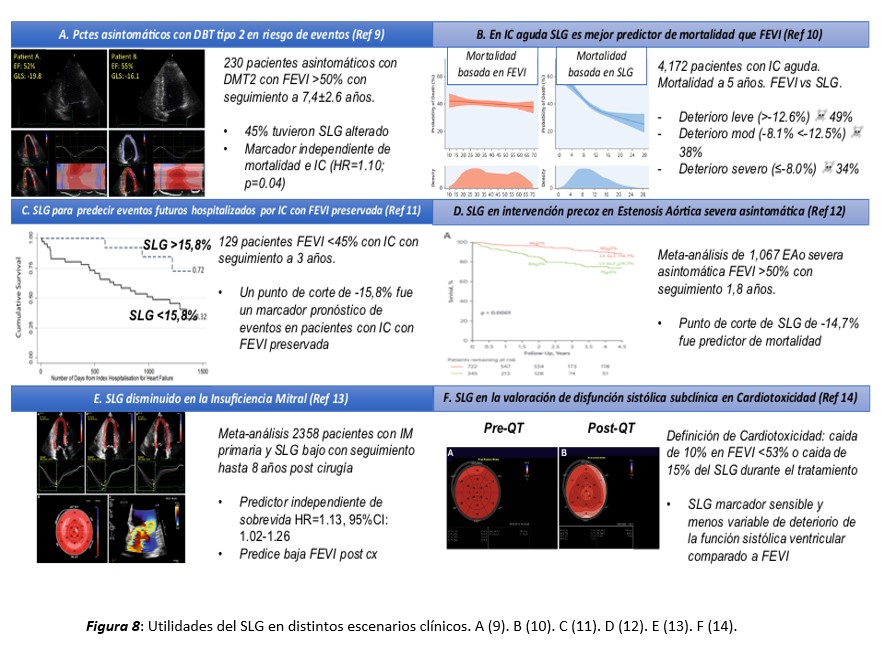
El SLG además ha sido estudiado en distintos escenarios clínicos, mostrando utilidad en el pronóstico de los pacientes y es planteado como un parámetro que puede ser determinante en la toma de decisiones quirúrgicas como el caso de las valvulopatías, estudios adicionales controlados y randomizados son requeridos para confirmar los datos de estudios observacionales. La Figura 8 resume las principales utilidades clínicas a la fecha del SLG en distintos tipos de pacientes.
Conclusiones:
La FEVI es el parámetro de función sistólica más comunmente utilizado para la toma de conductas en la práctica clínica, a pesar de eso tiene muchas limitaciones; de método, dada la no despreciable variabilidad para su estimación especialmente mediante la ecocardiografía bidimensional, y por otro lado, por su incapacidad para el diagnóstico y estratificación pronóstica del riesgo de eventos en escenarios clínicos como la IC con FEVI preservada o en enfermedades valvulares. El strain miocárdico propone ser la alternativa y el SLG es la técnica más estudiada para una aproximación etiológica de distintos patrones más específicos de enfermedades que pueden beneficiarse de terapias dirigidas y paramétros que permitan determinar el pronóstico por encima del valor de la FEVI. Necesitaremos de estudios adicionales que permitan establecer una estandarización entre distintas marcas y equipos con puntos de corte establecidos de valores normales y patológicos que nos permitan una mayor acogida en la práctica habitual.
Ver link AQUI
Blbliografía
1.Halliday BP, Senior R, Pennell DJ. Assessing left ventricular systolic function: from ejection fraction to strain analysis. Eur Heart J [Internet]. 2020 Sep 25; Available from: https://doi.org/10.1093/eurheartj/ehaa587
2.null null, Gregory HW, A. BD, Paul FJ, D. FS, A. FM, et al. ACCF/ACR/AHA/NASCI/SCMR 2010 Expert Consensus Document on Cardiovascular Magnetic Resonance. Circulation [Internet]. 2010 Jun 8;121(22):2462–508. Available from: https://doi.org/10.1161/CIR.0b013e3181d44a8f
3.Mor-Avi V, Jenkins C, Kühl HP, Nesser H-J, Marwick T, Franke A, et al. Real-Time 3-Dimensional Echocardiographic Quantification of Left Ventricular Volumes: Multicenter Study for Validation With Magnetic Resonance Imaging and Investigation of Sources of Error. JACC Cardiovasc Imaging [Internet]. 2008;1(4):413–23. Available from: http://www.sciencedirect.com/science/article/pii/S1936878X08001654
4.Rigolli M, Anandabaskaran S, Christiansen JP, Whalley GA. Bias associated with left ventricular quantification by multimodality imaging: a systematic review and meta-analysis. Open Hear [Internet]. 2016 Apr 27;3(1):e000388–e000388. Available from: https://pubmed.ncbi.nlm.nih.gov/27158524
5.Gorodezky M, Scott AD, Ferreira PF, Nielles-Vallespin S, Pennell DJ, Firmin DN. Diffusion tensor cardiovascular magnetic resonance with a spiral trajectory: An in vivo comparison of echo planar and spiral stimulated echo sequences. Magn Reson Med [Internet]. 2018;80(2):648—654. Available from: https://doi.org/10.1002/mrm.27051
6.D. SD, M. SH, P. PD, JOHN R, H. SE. Fiber Orientation in the Canine Left Ventricle during Diastole and Systole. Circ Res [Internet]. 1969 Mar 1;24(3):339–47. Available from: https://doi.org/10.1161/01.RES.24.3.339
7.Nakatani S. Left ventricular rotation and twist: why should we learn? J Cardiovasc Ultrasound [Internet]. 2011/03/31. 2011 Mar;19(1):1–6. Available from: https://pubmed.ncbi.nlm.nih.gov/21519484
8.Stokke TM, Hasselberg NE, Smedsrud MK, Sarvari SI, Haugaa KH, Smiseth OA, et al. Geometry as a Confounder When Assessing Ventricular Systolic Function: Comparison Between Ejection Fraction and Strain. J Am Coll Cardiol. 2017 Aug;70(8):942–54.
9.Holland DJ, Marwick TH, Haluska BA, Leano R, Hordern MD, Hare JL, et al. Subclinical LV dysfunction and 10-year outcomes in type 2 diabetes mellitus. Heart. 2015 Jul;101(13):1061–6.
10.Park JJ, Park J-B, Park J-H, Cho G-Y. Global Longitudinal Strain to Predict Mortality in Patients With Acute Heart Failure. J Am Coll Cardiol. 2018 May;71(18):1947–57.
11.Huang W, Chai SC, Lee SGS, MacDonald MR, Leong KTG. Prognostic Factors After Index Hospitalization for Heart Failure With Preserved Ejection Fraction. Am J Cardiol [Internet]. 2017;119(12):2017—2020. Available from: https://doi.org/10.1016/j.amjcard.2017.03.032
12.Magne J, Cosyns B, Popescu BA, Carstensen HG, Dahl J, Desai MY, et al. Distribution and Prognostic Significance of Left Ventricular Global Longitudinal Strain in Asymptomatic Significant Aortic Stenosis: An Individual Participant Data Meta-Analysis. JACC Cardiovasc Imaging. 2019 Jan;12(1):84–92.
13.Canessa M, Thamman R, Americo C, Soca G, Dayan V. Global longitudinal strain predicts survival and left ventricular function after mitral valve surgery. A meta-analysis. Semin Thorac Cardiovasc Surg. 2020 Sep;
14.Plana JC, Galderisi M, Barac A, Ewer MS, Ky B, Scherrer-Crosbie M, et al. Expert consensus for multimodality imaging evaluation of adult patients during and after cancer therapy: A report from the American society of echocardiography and the European association of cardiovascular imaging. Journal of the American Society of Echocardiography. 2014.









































Deje un comentario
Registrese para comentar. Sus e-mail no será publicados